Синдром слабости синусового узла
При сборе жалоб и анамнеза у пациентов с синдромом слабости синусового узла (СССУ) необходимо определить:
- Клинические проявления СССУ, включая наличие обмороков и предобморочных состояний, а также обстоятельства их возникновения.
- Возможные причины СССУ: перенесённый инфаркт миокарда, миокардит, операции на сердце, приём антиаритмических препаратов, семейный анамнез (брадикардия, имплантированные ЭКС у родственников), занятия спортом, храп во сне и др.
- Сочетание с другими нарушениями ритма и проводимости, особенно с фибрилляцией предсердий (ФП).
При физическом обследовании выявляют брадикардию в покое или при физической нагрузке, аритмичные тоны сердца (экстрасистолия, паузы ритма), различные виды тахикардий при синдроме брадикардии-тахикардии. Стойкая брадикардия может приводить к компенсаторному повышению артериального давления (гемодинамическая артериальная гипертензия).
У пациентов с ваготонической дисфункцией синусового узла могут наблюдаться признаки ваготонии (гипергидроз, стойкий красный дермографизм, мраморность ладоней) и симптомы мезенхимальной дисплазии (астеническая конституция, гипермобильность суставов, плоскостопие, систолический шум при пролапсе митрального клапана).
Необходимы следующие исследования:
- Общий анализ крови (гемоглобин, лейкоциты, СОЭ).
- Определение липидного спектра, уровня тироксина и тиреотропного гормона.
- При подозрении на миокардит — электрофорез белков, определение С-реактивного белка, фибриногена, сердечных тропонинов T или I, креатинкиназы, антител к миокарду и кардиотропным вирусам (Коксаки, цитомегаловирус, вирус Эпштейна-Барр, вирусы группы герпеса), стрептококкам.
- Генетическое обследование при подозрении на генетически детерминированное заболевание как причину СССУ.
Стандартное электрокардиографическое исследование в 12 отведениях
Диагностика СССУ с помощью ЭКГ в 12 отведениях ограничена, так как аритмия часто носит преходящий характер. Тем не менее, существуют критерии для диагноза СССУ:
- Постоянная синусовая брадикардия в течение суток с частотой сердечных сокращений (ЧСС) менее 50 в минуту.
- Синусовые паузы более 3 секунд, вызванные различными причинами.
- Синоатриальная блокада II степени:
- Первого типа — постепенное укорочение интервала Р-Р с последующим резким удлинением (обратная периодика Самойлова-Венкебаха).
- Второго типа — пауза ритма, кратная предшествующему интервалу Р-Р.
- Остановка синусового узла — пауза, не кратная предшествующим интервалам Р-Р.
- Удлинённая постэкстрасистолическая пауза (компенсаторная пауза после экстрасистолы превышает два интервала R-R). Снижение ЧСС после экстрасистолы называется постэкстрасистолической депрессией синусового ритма. Аналогичный феномен может наблюдаться и после пароксизма тахикардии. Пауза перед восстановлением синусового ритма более 1,5 секунд может указывать на латентный СССУ. Во время пауз могут появляться замещающие ритмы (предсердные, узловые, желудочковые) различной продолжительности.
Длительные или интермиттирующие периоды замещающих ритмов, сопровождающиеся клиническими симптомами.
Синдром брадикардии-тахикардии — чередование синусовой брадикардии и пауз с пароксизмами ФП (в 58% случаев) и/или предсердной тахикардией, особенно когда наблюдается возвращение к редкому синусовому ритму после наджелудочковой тахикардии. Такие эпизоды могут возникать десятки раз в сутки и купироваться спонтанно.
Холтеровское мониторирование
Холтеровское мониторирование ЭКГ позволяет фиксировать вышеуказанные ЭКГ-признаки и соотносить их с клиническими проявлениями.
Нагрузочные ЭКГ-пробы
Значимость нагрузочных тестов в диагностике СССУ невелика. Тредмил-тест позволяет определить прирост ЧСС в ответ на физическую нагрузку. Хронотропная недостаточность проявляется отсутствием прироста ЧСС более 90-100 в минуту при повседневной и выше 110-120 в минуту при значительной физической нагрузке. Нагрузочные тесты также помогают исключить или подтвердить, что ишемическая болезнь сердца является причиной нарушений ритма.
Эхокардиография
ЭхоКГ позволяет выявить морфологические и функциональные изменения сердца (клапанные дефекты, гипертрофия левого желудочка, фракция выброса, наличие зон гипо- и акинезии, увеличение полостей сердца), что может указывать на заболевание, являющееся причиной аритмии.
Чреспищеводное и внутрисердечное электрофизиологическое исследование сердца
При отсутствии убедительных критериев диагноза по данным мониторирования ЭКГ диагноз СССУ можно подтвердить с помощью электрофизиологического исследования, чаще чреспищеводного. Определяются:
- Время восстановления функции синусового узла — интервал между последним стимулом и первым синусовым зубцом Р (норма — не более 1500-1600 мс).
- Корригированное время восстановления функции синусового узла — разность между временем восстановления функции синусового узла и спонтанным сердечным циклом до стимуляции (норма — не более 525-600 мс).
Специфичность этих показателей в диагностике СССУ составляет более 90%, чувствительность — 45-85%.
Дифференциальную диагностику следует проводить между СССУ органической природы и ваготонической дисфункцией синусового узла. У молодых людей до 20 лет ваготония может быть вариантом нормы. Брадикардия, миграция водителя ритма и паузы, наблюдаемые ночью, чередуются с адекватным или избыточным приростом ЧСС при физических нагрузках. Ваготоническую дисфункцию синусового узла диагностируют при выраженных ЭКГ-признаках дисфункции, часто в сочетании с клинической картиной нейроциркуляторной дистонии по ваготоническому типу.
При нормализации увеличенных времени восстановления функции синусового узла и корригированного времени восстановления функции синусового узла диагностируют ваготоническую дисфункцию, а при сохранении или усугублении признаков нарушения автоматизма — СССУ органической природы.
У пациентов с синдромом ночного апноэ связь нарушений сердечного ритма с эпизодами десатурации возможно подтвердить при одновременном мониторировании ЭКГ и пульс-оксиметрии.
Обследование и лечение пациентов с головокружением и обмороками в анамнезе, а также с признаками дисфункции синусового узла представляет наибольшие трудности. Не всегда ясно, является ли дисфункция причиной этих симптомов.
При ведении пациентов с ваготонической дисфункцией синусового узла может быть полезно участие невролога, психиатра или психотерапевта. При показаниях к имплантации ЭКС необходима консультация кардиохирурга.
В формулировке диагноза следует указывать основное заболевание, вид нарушений автоматизма и наиболее важные клинические проявления.
Первичный синдром возникает при органических поражениях синоатриальной зоны:
- Гипертоническая болезнь, миокардиты, ишемическая болезнь сердца, пороки сердца.
- Инфильтративные и идиопатические дегенеративные патологии.
- Злокачественные опухоли сердца, гипертиреоз, старческий амилоидоз и др.
Первичный синдром может быть обусловлен внешними факторами, такими как:
- Приём определённых лекарств.
- Гиперкальциемия.
- Гиперкалиемия и др.
Тонус блуждающего нерва может повышаться во время сна, при кашле, дефекации, мочеиспускании, тошноте и рвоте. Патологическая активация нерва возможна при заболеваниях пищеварительной системы, болезнях глотки и других процессах.
Формы заболевания
Выделяют четыре формы заболевания:
- Латентная. Характеризуется отсутствием клинических и ЭКГ-симптомов. Дисфункция обычно выявляется при электрофизиологических исследованиях.
- Компенсированная. Может проявляться в виде брадисистолического и брадитахисистолического вариантов. Первый вариант сопровождается слабыми симптомами, такими как слабость и головокружение. Второй вариант включает пароксизмальные тахиаритмии.
- Декомпенсированная. Также имеет две формы. Первая сопровождается нарушением кровотока, головокружением и обмороками, что ограничивает трудоспособность. Вторая форма приводит к полной нетрудоспособности пациента.
- Постоянная. Протекает в двух вариантах, при этом пациент ограничен в трудоспособности. Во втором варианте, при наличии сердечной недостаточности и церебральной симптоматики, устанавливается электрокардиостимулятор.
Любая из форм дисфункции может предшествовать развитию мерцательной аритмии.
Симптомы патологии
Длительное время патология может протекать бессимптомно.
Для слабости синусового узла характерны следующие признаки:
- нарушения сердечного ритма (брадикардия);
- головные боли;
- головокружение;
- постоянная усталость;
- резкая слабость;
- ощущение замирания или остановки сердца;
- эмоциональная лабильность.
У пожилых пациентов часто наблюдаются снижение интеллекта и памяти.
При прогрессировании патологии могут возникнуть нарушения со стороны желудочно-кишечного тракта.
Заболевание имеет тенденцию к прогрессированию. Симптомы усугубляются при отсутствии лечения. Внезапная сердечная смерть может наступить на любой стадии патологии. Продолжительность жизни пациентов варьируется от нескольких недель до 10 и более лет и зависит от множества факторов. Своевременное обращение к специалисту может помочь сохранить здоровье и жизнь.
Диагностика
Синдром слабого синусового узла
Синдром слабости синусового узла (СССУ, синдром дисфункции синусового узла) — это нарушение ритма, вызванное ослаблением или прекращением функции автоматизма синусно-предсердного узла.
При СССУ нарушается образование и проведение импульсов из синусового узла в предсердия, что приводит к брадикардии и эктопическим аритмиям. У пациентов с этим синдромом возможна внезапная остановка сердечной деятельности.
Синдромом слабости синусового узла чаще страдают пожилые люди (старше 60-70 лет) обоего пола, хотя он также встречается у детей и подростков. Распространенность СССУ в общей популяции составляет от 0,03 до 0,05%.
Существуют вегетативные и медикаментозные нарушения функции автоматизма, которые устраняются лекарственной денервацией сердца или отменой препаратов, подавляющих образование и проведение импульсов.
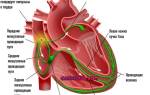
Синусовый узел, расположенный в зоне устья верхней полой вены в правом предсердии, является генератором импульсов и водителем сердечного ритма. В норме он генерирует электрические импульсы с частотой 60—80 в минуту.
Синусовый узел состоит из ритмогенных пейсмекерных клеток, обеспечивающих автоматизм. Его деятельность регулирует вегетативная нервная система, что проявляется изменениями сердечного ритма в зависимости от гемодинамических потребностей организма: учащение при физической нагрузке и замедление в покое.
При синдроме слабости синусового узла может наблюдаться периодическая или постоянная утрата синусно-предсердным узлом ведущей роли в формировании сердечного ритма.
-
Латентная форма — отсутствие клинических и ЭКГ-симптомов; дисфункция определяется при электрофизиологическом исследовании. Ограничений трудоспособности нет; имплантация электрокардиостимулятора не показана.
-
Компенсированная форма:
- Брадисистолический вариант — слабо выраженные клинические проявления, такие как головокружение и слабость. Возможны профессиональные ограничения; имплантация электрокардиостимулятора не показана.
- Брадитахисистолический вариант — к симптомам брадисистолического варианта добавляются пароксизмальные тахиаритмии. Имплантация электрокардиостимулятора показана при декомпенсации синдрома под влиянием противоаритмической терапии.
-
Декомпенсированная форма:
- Брадисистолический вариант — стойкая синусовая брадикардия; проявляется нарушением церебрального кровотока (головокружение, обмороки, преходящие парезы), сердечной недостаточностью. Значительное ограничение трудоспособности; показания к имплантации — асистолия и время восстановления функции синусового узла (ВВФСУ) более 3 секунд.
- Брадитахисистолический вариант (синдром Шорта) — к симптомам брадисистолического варианта добавляются пароксизмальные тахиаритмии. Пациенты полностью нетрудоспособны; показания к имплантации те же, что и при брадисистолическом варианте.
-
Постоянная брадисистолическая форма мерцательной аритмии (на фоне ранее диагностированного синдрома слабости синусового узла):
- Тахисистолический вариант — ограничение трудоспособности; показаний к имплантации нет.
- Брадисистолический вариант — ограничение трудоспособности; показаниями к имплантации служат церебральная симптоматика и сердечная недостаточность.
Развитию брадисистолической формы мерцательной аритмии может предшествовать любая из форм дисфункции синусового узла.
В зависимости от регистрации признаков слабости синусового узла при холтеровском ЭКГ-мониторировании выделяют латентное (признаки СССУ не выявляются), интермиттирующее (признаки выявляются при снижении симпатического и увеличении парасимпатического тонуса, например, в ночные часы) и манифестирующее течение (признаки выявляются при каждом суточном ЭКГ-мониторировании).
Синдром слабости синусового узла может протекать остро и хронически, с рецидивами. Острое течение часто наблюдается при инфаркте миокарда.
По этиологическим факторам различают первичную и вторичную формы синдрома. Первичная форма вызывается органическими поражениями синусно-предсердной зоны, вторичная — нарушением ее вегетативной регуляции.
К первичному синдрому относятся дисфункции, вызванные органическими поражениями синоатриальной зоны при:
- кардиальной патологии — ИБС, гипертонической болезни, кардиомиопатии, пороках сердца, миокардитах, хирургических травмах и трансплантации сердца;
- идиопатических дегенеративных и инфильтративных заболеваниях;
- гипотиреозе, дистрофии костно-мышечного аппарата, старческом амилоидозе, саркаидозе, злокачественных опухолях сердца, в стадии третичного сифилиса и др.
Ишемия, вызванная стенозом артерии, питающей синусовый узел, воспаление, инфильтрация, кровоизлияние, дистрофия, локальный некроз, интерстициальный фиброз и склероз приводят к замещению функциональных клеток синусно-предсердного узла соединительной тканью.
Вторичный синдром обусловлен экзогенными факторами, воздействующими на синусный узел, такими как гиперкалиемия, гиперкальциемия и лечение препаратами, снижающими автоматизм (β-адреноблокаторы, клофелин, допегит, резерпин, кордарон, верапамил, сердечные гликозиды и др.).
Особо выделяют вегетативную дисфункцию синусового узла (ВДСУ), часто наблюдаемую при гиперактивации блуждающего нерва, что вызывает урежение синусового ритма и удлинение рефрактерности узла.
Тонус блуждающего нерва может повышаться при физиологических процессах: во сне, мочеиспускании, дефекации, кашле, глотании, тошноте и рвоте, пробе Вальсавы.
Патологическая активация может быть связана с заболеваниями глотки, мочеполового и пищеварительного трактов, а также при гипотермии, гиперкалиемии, сепсисе, повышении внутричерепного давления.
ВДСУ чаще наблюдается у подростков и молодых людей из-за значительной невротизации.
У спортсменов может развиваться истинная СССУ в сочетании с другими нарушениями ритма, обусловленными дистрофией миокарда.
Клинические проявления синдрома варьируют. У некоторых пациентов симптомы могут отсутствовать длительное время, у других — наблюдаются выраженные нарушения ритма, головные боли, головокружение, приступы Морганьи-Адамса-Стокса.
Возможны расстройства гемодинамики из-за уменьшения ударного и минутного объема, что может привести к кардиальной астме, отеку легких, коронарной недостаточности (стенокардии, реже — инфаркту миокарда).
В клинике СССУ выделяют две основные группы симптомов: церебральные и кардиальные. Церебральная симптоматика при маловыраженных нарушениях ритма проявляется усталостью, раздражительностью, забывчивостью, эмоциональной лабильностью. У пожилых пациентов может наблюдаться снижение интеллекта и памяти.
При прогрессировании СССУ и недостаточности мозгового кровообращения церебральные симптомы усиливаются. Развиваются предобморочные состояния и обмороки, предшествующие шумом в ушах, резкой слабостью, ощущением замирания сердца.
Обмороки кардиального генеза при синдроме Морганьи-Эдемс-Стокса протекают без предвестников и судорог (исключение — длительная асистолия).
Кожные покровы бледнеют, холодеют, покрываются потом, АД резко снижается. Обмороки могут провоцироваться кашлем, резким поворотом головы, тесным воротником.
Выраженная брадикардия может вызывать дисциркуляторную энцефалопатию, проявляющуюся головокружением, провалами в памяти, парезами, раздражительностью, инсомнией.
Кардиальные проявления начинаются с ощущений замедленного или нерегулярного пульса, болей за грудиной из-за недостатка коронарного кровотока. Присоединяющиеся аритмии сопровождаются сердцебиением, перебоями в работе сердца, одышкой, слабостью, развитием хронической сердечной недостаточности.
При прогрессировании СССУ может развиваться вентрикулярная тахикардия или фибрилляция, что увеличивает риск внезапной сердечной смерти.
Среди других органических проявлений могут отмечаться олигурия, обусловленная почечной гипоперфузией; нарушения со стороны ЖКТ, перемежающаяся хромота, мышечная слабость из-за недостаточности оксигенации внутренних органов и мышц.
Источник: gig-games.ru
https://youtube.com/watch?v=4JbXHzEPTTA
С СИНДРОМОМ СЛАБОСТИ СИНУСОВОГО УЗЛА
Оглавление
- Методология
- Определение
- Коды МКБ 10
- Эпидемиология
- Этиология
- Патогенез
- Классификация
- Клиническая картина
- Диагностика
- Примеры диагнозов
- Лечение
- Ведение пациентов
- Профилактика
- Исходы и прогноз
Федеральные клинические рекомендации по оказанию медицинской помощи детям с синдромом слабости синусового узла подготовлены Ассоциацией детских кардиологов России и утверждены на ………………
Рабочая группа:
- Школьникова М.А., д.м.н., профессор
- Ковалёв И.А., д.м.н., профессор
- Полякова Е.Б., к.м.н.
- Березницкая В.В., к.м.н.
- Термосесов С.А.
- Чернышёва Т.В., к.м.н.
- Балыкова Л.А., д.м.н., профессор
МЕТОДОЛОГИЯ
Методы сбора и селекции доказательств: поиск в электронных базах данных.
Описание методов оценки качества и силы доказательств: основой для рекомендаций служат публикации из Кохрейновской библиотеки, а также базы данных EMBASE, MEDLINE и PubMed. Глубина поиска составляет 5 лет.
Методы оценки качества и силы доказательств:
- консенсус экспертов;
- оценка значимости по рейтинговой схеме.
Методы анализа доказательств:
- обзоры опубликованных мета-анализов;
- систематические обзоры с таблицами доказательств.
При отборе публикаций для анализа методология каждого исследования изучается для проверки валидности. Результаты этого анализа влияют на уровень доказательств, присваиваемый публикации, что, в свою очередь, сказывается на силе рекомендаций.
Для минимизации ошибок каждое исследование оценивалось независимо. Все различия в оценках обсуждались группой авторов. При отсутствии консенсуса привлекался независимый эксперт.
Таблицы доказательств заполнялись авторами клинических рекомендаций.
Методы формулирования рекомендаций: консенсус экспертов.
Индикаторы доброкачественной практики (Good Practice Points – GPPs) основываются на клиническом опыте авторов рекомендаций.
Экономический анализ: анализ стоимости не проводился, публикации по фармакоэкономике не анализировались.
Методы валидизации рекомендаций: внешняя и внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Популяция имеет электрофизиологические особенности, предрасполагающие к нарушениям функции синусового узла под воздействием неблагоприятных факторов. Распространенность этих нарушений в детском возрасте достигает 0,84% среди пациентов с кардиальной патологией.
Среди практически здоровых детей признаки дисфункции синусового узла на стандартной электрокардиограмме (ЭКГ) выявляются у 2% детей. Синусовая брадикардия — наиболее частая (до 85%) форма брадиаритмий у детей.
По данным популяционного ЭКГ-скрининга в России, распространенность миграции ритма составляет 1,9%, выскальзывающих и замещающих наджелудочковых ритмов — 0,7%, а синоатриальной блокады — 0,3%.
Холтеровское мониторирование (ХМ) показывает более высокую распространенность ЭКГ-феноменов, связанных с синдромом слабости синусового узла (СССУ). У 19% детей первого года жизни отмечаются выскальзывающие и замещающие идиовентрикулярные ритмы, у 7% — эпизоды остановки синусового узла, у 11% — синоатриальные блокады. Среди практически здоровых детей старшего возраста признаки дисфункции синусового узла встречаются в 2,7% случаев. У детей с брадиаритмиями синоатриальные блокады наблюдаются в 50% случаев. В хирургических клиниках СССУ связывают с около 10% всех нарушений сердечного ритма, а на долю СССУ приходится до 30% всех аритмий у детей.
ЭТИОЛОГИЯ
Синдром слабости синусового узла (СССУ) у взрослых чаще всего имеет ишемический характер и проявляется мерцательной аритмией. У детей СССУ обычно развивается без органической патологии сердечно-сосудистой системы. Нарушения ритма у детей могут быть вызваны различными факторами, такими как вегетативный дисбаланс с преобладанием парасимпатических влияний, медикаментозное воздействие, воспаление миокарда, обменные нарушения и аутоиммунные реакции на проводящую систему сердца.
По этиологическим факторам выделяют:
-
СССУ органической природы (при кардиомиопатиях, амилоидозе, саркоидозе, коллагенозах, ишемической болезни сердца, опухолях сердца, гормонально-обменных кардиотоксических нарушениях и др.).
-
Регуляторные (вагусные) дисфункции синусового узла (вегетососудистая дистония с преобладанием парасимпатических влияний, гиперваготония при повышении внутричерепного давления, отеке мозга, вазовагальные рефлексы при органной патологии).
-
СССУ как следствие токсических влияний (антиаритмические препараты, сердечные гликозиды, антидепрессанты, снотворные средства, отравления карбофосом и другими веществами, блокирующими холинэстеразу).
-
Нарушение функции синусового узла у детей после операций на сердце (коррекция врожденных пороков, таких как транспозиция магистральных сосудов, дефект межпредсердной перегородки и др.).
-
Врожденное нарушение функции синусового узла.
-
Аутоиммунные нарушения функции синусового узла.
-
Идиопатические случаи (причина не установлена).
В первых четырех случаях речь идет о вторичном СССУ, устранение которого зависит от эффективности лечения основного заболевания. В детской кардиологии часто не удается выявить заболевание, приводящее к нарушению функции синусового узла, что позволяет говорить о первичном или идиопатическом варианте. Порой сложно провести грань между органическими и функциональными изменениями без морфологического подтверждения.
ПАТОГЕНЕЗ
Среди патогенетических механизмов идиопатического СССУ выделяют влияние вегетативной нервной системы, дегенеративные изменения, апоптоз и воспалительное поражение миокарда.
Недостаточность симпатических влияний на сердце доказана как фактор, способствующий прогрессирующему нарушению функции синусового узла у детей. В формировании нарушений вегетативной регуляции сердца важную роль играют гипоксические поражения в перинатальном и раннем неонатальном периодах.
Роль центральной нервной системы в дисфункции синусового узла подтверждена экспериментально. Сердечный ритм формируется в результате взаимодействия центральных нервных импульсов, проходящих по блуждающим нервам к сердцу, и пейсмекерной активности синусового узла. Таким образом, ритм сердца определяется иерархией механизмов, включая мозговой и внутрисердечный уровни. В эксперименте была создана модель СССУ, где прогрессирующее нарастание электрокардиографических изменений связано с ослаблением влияния центральной нервной системы на ритмогенез. На первой стадии наблюдается миграция ритма, на второй — выскальзывающие сокращения, на третьей — синдром тахикардии-брадикардии. Максимальное снижение функциональной активности синусового узла происходит при значительном снижении центральных влияний и проявляется ригидной брадикардией.
Вопрос о роли аутоиммунных механизмов в развитии и прогрессировании СССУ активно обсуждается. Повышение титров антикардиальных антител у пациентов с выраженным поражением синусового узла, наряду с вегетативной дисфункцией, может быть одним из звеньев патогенеза синдрома у детей.
Подтверждена также роль генетических механизмов в развитии СССУ. Описаны аутосомно-доминантный и аутосомно-рецессивный типы наследования дисфункций синусового узла, а также полиморфизмы генов HCN1-4, SCN5A и KCNE, ответственные за развитие СССУ. Наличие мутаций может предрасполагать к дисфункции синусового узла или повышать чувствительность клеток синусового узла к препаратам, влияющим на частоту сердечных сокращений.
Таким образом, идиопатический СССУ у детей можно рассматривать как результат медленно прогрессирующего дегенеративного поражения проводящей системы сердца, при этом наиболее ранние и выраженные изменения касаются иннервации синусового узла. Наследственная предрасположенность может способствовать как формированию вегетативной патологии, так и первичным электрофизиологическим изменениям проводящей системы сердца.
КЛАССИФИКАЦИЯ
У детей выделяют четыре клинико-электрокардиографических варианта нарушения функции синусового узла (табл. 1). Первый вариант включает минимальные проявления, такие как синусовая брадикардия и миграция ритма. Второй вариант характеризуется замещающими ритмами, остановками синусового узла и синоатриальной блокадой на фоне более выраженной депрессии основного ритма. Третий вариант (синдром тахи-брадикардии) представляет собой сочетание синусовой брадикардии с суправентрикулярной гетеротопной тахикардией. Четвертый вариант включает кардионейропатию с выраженной брадикардией, множеством замещающих ритмов, асистолиями и нарушением реполяризации миокарда.
Каждый из этих вариантов часто сопровождается нарушениями АВ проведения. Наблюдается стадийность формирования нарушений функции синусового узла у детей: от первого варианта ко второму (или третьему, в зависимости от наличия условий для тахиаритмий) и далее к четвертому варианту.
КЛИНИЧЕСКАЯ КАРТИНА
Клинические симптомы синдрома слабости синусового узла (СССУ) у детей не специфичны и могут отсутствовать. Чаще всего дети жалуются на головокружение, плохую переносимость физических нагрузок, утомляемость и эпизоды слабости.
Наиболее серьезными проявлениями СССУ являются аритмогенные обморочные состояния (приступы Морганьи-Адамса-Стокса) и внезапная сердечная смерть.
У детей с начальными проявлениями СССУ могут наблюдаться рефлекторные обморочные состояния, возникающие из-за резкого падения общего периферического сосудистого сопротивления или артериального давления. Аритмогенные обмороки чаще встречаются у детей с III и IV вариантами заболевания. Как при нейрокардиогенных, так и при аритмогенных синкопальных состояниях действуют схожие патофизиологические механизмы: недостаточная симпатическая стимуляция и активация парасимпатической нервной системы, что приводит к расширению сосудов, депонированию крови в венах и снижению венозного возврата. В этих случаях потеря сознания связана с недостаточностью функции синусового узла и зависит от чувствительности центральной нервной системы к гипоксии. В кардиологической практике для развития потери сознания у взрослых необходимо внезапное урежение частоты сердечных сокращений на 20 уд/мин или асистолия не менее 5 секунд. У детей с нарушениями сердечного ритма четкой взаимосвязи между длительностью асистолии и клиническими проявлениями не установлено.
ДИАГНОСТИКА
Сбор анамнеза у пациентов с синдромом слабости синусового узла (СССУ) крайне важен. Он должен включать информацию о наличии и степени брадикардии на ретроспективных ЭКГ, анализ ЭКГ родственников на предмет наследственной брадикардии, а также клинические данные: наличие жалоб на предобморочные и обморочные состояния, возраст их появления, связь с перенесенными заболеваниями, провоцирующие факторы, наличие ауры, судорог и непроизвольного мочеиспускания во время синкопе, субъективные ощущения до и после обморока, частоту сердечных сокращений (ЧСС) и артериальное давление (АД) во время обморока, длительность синкопе и особенности их купирования.
Основным методом диагностики СССУ является электрокардиография. Электрокардиографические критерии синусовой брадикардии представлены в таблице 2. Брадикардией в различных возрастных группах считается снижение ЧСС ниже 5-го перцентиля возрастного распределения. Более обоснованным критерием является снижение ниже 2-го перцентиля, что у детей данного возраста связано с высоким риском развития СССУ и синкопальных состояний.
Холтеровское мониторирование (ХМ) ЭКГ — наиболее эффективный метод диагностики и оценки лечения детей с нарушениями функции синусового узла. Важным аспектом является оценка минимальной ЧСС при ХМ (таблица 3). Степень снижения средней ЧСС в дневное и ночное время помогает дифференцировать патологическую и физиологическую брадикардию. Для физиологической брадикардии характерно снижение ЧСС в ночное время, в то время как средняя дневная и суточная ЧСС остаются в пределах нормы. ХМ также используется для диагностики аритмий, метаболических изменений в миокарде, оценки вариабельности ритма и вегетативных влияний на сердечный ритм, а также выявления маркеров риска жизнеугрожающих состояний и оценки эффективности лечения.
На ЭКГ детей с СССУ, помимо синусовой брадикардии, могут наблюдаться различные наджелудочковые тахиаритмии (тахикардии, фибрилляция предсердий, экстрасистолия). Миграция водителя ритма и замещающие сокращения возникают из-за ослабления функции синусового узла и являются вторичными. Ускоренный суправентрикулярный ритм также может встречаться у детей, что требует исключения синдрома слабости синусового узла по типу тахи-брадикардии.
Синоатриальная блокада может быть вызвана как усилением парасимпатических влияний, так и органическими причинами, такими как нарушение кровообращения в перинодальной области. Она различается по степени тяжести: первая степень характеризуется замедлением проведения возбуждения, вторая — блокировкой некоторых импульсов, третья — нарушением проведения импульсов к миокарду правого предсердия.
Остановка синусового узла (синус-арест) — это потеря способности генерации импульсов, возникающая из-за нарушения 4-й фазы деполяризации в пейсмекерных клетках. При этом развивается пауза ритма, превышающая предшествующий интервал R-R более чем в 2 раза.
Регистрация ЧСС в момент появления клинической симптоматики у пациентов с синкопальными состояниями имеет важное значение. Повторное длительное ЭКГ мониторирование для выявления нарушений ритма как причины синкопе более информативно, чем однократное 24-часовое ХМ. Оптимальным решением является имплантация петлевых регистраторов, которые позволяют мониторировать ЧСС в течение трех лет. Во время обморока может развиться критическая брадикардия или асистолия, даже при отсутствии признаков нарушения функции синусового узла вне приступа. «Золотым стандартом» диагностики синкопальных состояний остается регистрация ЭКГ в момент появления симптомов.
Электрофизиологические исследования также применяются для диагностики дисфункций синусового узла. Чреспищеводная электростимуляция позволяет оценить функцию синусового узла. Проба оценивает время восстановления функции синусового узла (ВВФСУ) и скорректированное время восстановления (КВВФСУ). Если показатели превышают норму, это свидетельствует о снижении автоматической активности синусового узла.
Нормативные значения электрофизиологических показателей функции синусового узла в различных возрастных категориях детей представлены в таблице 5. Наличие нормальных значений параметров чреспищеводной электростимуляции не исключает дисфункцию синусового узла.
Внутрисердечное электрофизиологическое исследование изучает активность синусового узла через запись электрограммы. Однако эта высокозатратная методика не обладает высокой специфичностью и чувствительностью, что ограничивает ее прогностическую ценность.
ЭХО-кардиография с доплеровским анализом и цветным картированием проводится для исключения органической патологии сердца и оценки морфометрических показателей.
Лабораторная диагностика важна для определения этиологии СССУ. Клинический анализ крови и мочи помогает исключить воспалительные изменения. Оцениваются уровни электролитов, маркеров повреждения миокарда, липидного спектра и активности ферментов. Для исключения вторичного генеза брадикардий исследуется уровень гормонов щитовидной железы.
Иммунологическое исследование включает определение уровня специфических антител к антигенам проводящей системы сердца и кардиомиоцитам. Молекулярно-генетический анализ используется для выявления мутаций, вызывающих брадикардию. Также могут проводиться исследования на наличие хронической очаговой инфекции.
Для дифференциальной диагностики СССУ и вегетативных дисфункций применяются дополнительные пробы. Простейшей нагрузочной пробой является активный ортостаз или 10 приседаний с последующим снятием стандартной ЭКГ. Нормальная реакция — увеличение ЧСС на 10-15%. Недостаточный прирост ЧСС или появление нарушений ритма свидетельствует о наличии СССУ.
Существуют различные методики динамических нагрузок, предпочтение в педиатрии отдается тредмил-тесту. Максимальная ЧСС у здоровых детей достигает 180-190 в минуту, в то время как у пациентов с СССУ — 100-120 в минуту. Критерием наличия СССУ может быть максимальная ЧСС менее 180 в минуту и неадекватное снижение ЧСС при прекращении нагрузки.
Для оценки влияния вегетативной нервной системы применяется активная клиноортостатическая проба. Нормальная реакция — отсутствие жалоб, увеличение ЧСС на 20-40% и кратковременный подъем АД. Патологические варианты пробы характеризуются избыточным или недостаточным вегетативным обеспечением.
Проба с атропином используется для устранения парасимпатических влияний. Вводится 0,1% раствор сульфата атропина, после чего оценивается прирост ЧСС. Нормальная реакция — устойчивый синусовый ритм с соответствующей возрасту ЧСС и приростом не менее 30%. Недостаточный прирост ЧСС указывает на наличие СССУ. Массаж каротидного синуса и проба Вальсальвы также помогают выявить активность парасимпатических влияний.
ПРИМЕРЫ ДИАГНОЗОВ
Синдром слабости синусового узла, II вариант: брадикардия, паузы ритма до 1900 мс, эпизоды остановки синусового узла, одиночные наджелудочковые выскальзывающие сокращения.
Синдром слабости синусового узла, IV вариант: ригидная брадикардия, 2-й идиовентрикулярный замещающий ритм, паузы ритма до 2500 мс, эпизоды остановки синусового узла.
ЛЕЧЕНИЕ
Медикаментозная терапия:
Критические ситуации, такие как головокружение и синкопальные состояния, вызванные брадикардией или асистолией, устраняются с помощью холинолитиков (атропин) и бета-адреномиметиков (изопреналин). Дозы препаратов для неотложной терапии СССУ указаны в таблице 6. Однако постоянное применение этих средств нежелательно, так как они угнетают активность синусового узла и увеличивают потребность миокарда в кислороде, что может привести к гипотензии и желудочковым аритмиям. При необходимости проводят непрямой массаж сердца и искусственное дыхание. Для купирования острых брадиаритмий может использоваться временная (чрескожная) электрокардиостимуляция.
При выраженном заместительном гетеротопном ритме с высокой частотой сердечных сокращений и аритмогенной дисфункцией миокарда у детей с синдромом тахи-брадикардии может потребоваться антиаритмическая терапия под контролем ЭКГ и ХМ. Антиаритмические препараты противопоказаны детям с синкопе в анамнезе, выраженным угнетением синусового узла, частыми паузами ритма и нарушениями АВ-проводимости. При остром начале заболевания, наличии воспалительных маркеров или подозрении на аутоиммунный генез воспалительных изменений при СССУ (высокие титры антикардиальных аутоантител 1:160 и выше) могут быть рекомендованы курсы нестероидных противовоспалительных препаратов (найз, ибупрофен) на 1-3 месяца и глюкокортикоидов в низких дозах (преднизолон, дексаметазон) не менее чем на 2 недели.
В лечении пациентов с СССУ может применяться стимулирующая терапия с широким спектром действия. Используются адаптогены и ноотропные средства – настойки женьшеня, элеутерококка, пирацетам, церебролизин, а также метаболические и мембраностабилизирующие препараты – коэнзим Q10, карнитин, милдронат, неотон. Длительное применение (до 6 месяцев) этих препаратов (не более 4-х одновременно) стимулирует окислительно-восстановительные процессы, повышает устойчивость мозга к гипоксии и стабилизирует клеточные мембраны. Стимуляция симпатического отдела вегетативной нервной системы с помощью вегетотропных препаратов может замедлить прогрессирование синдрома и восстановить нормальный ритм, что особенно важно для детей раннего возраста, у которых интервенционное лечение затруднено. Терапия, стимулирующая нейрогуморальные симпатические влияния на сердечный ритм, также может быть оправдана у пациентов с сопутствующими вегетативными дисфункциями.
Таблица 6. Лекарственные препараты, используемые в неотложной терапии пациентов с СССУ
Немедикаментозная терапия:
Имплантация электрокардиостимулятора (ЭКС) является наиболее эффективным методом коррекции пациентов с СССУ. Решение о необходимости и сроках имплантации, а также выборе режима стимуляции принимается индивидуально, с учетом возраста ребенка.
Контроль состояния пациента осуществляется по данным ЭКГ и ХМ, включая минимальную ЧСС, паузы ритма, сопутствующие нарушения и гемодинамические показатели по данным УЗИ сердца. Продолжительность госпитализации зависит от тяжести состояния, но не должна превышать 14 дней. При ухудшении брадикардии, увеличении пауз ритма или ухудшении гемодинамических показателей необходим контроль 1 раз в 3-6 месяцев для определения показаний к имплантации ЭКС. При появлении симптомов, связанных с брадикардией (утомляемость, головокружение, обмороки), проводится внеплановое обследование для определения показаний к имплантации. При наличии таковых пациент госпитализируется в кардиохирургическую клинику, имеющую опыт имплантации эпикардиальных и эндокардиальных систем ЭКС. Средняя продолжительность госпитализации при имплантации эпикардиальных систем составляет 14-21 день, при имплантации эндокардиальных систем – 10-14 дней.
Пациенты с имплантированным ЭКС наблюдаются каждые 6 месяцев в течение года после имплантации, затем ежегодно. Регулярное обследование включает оценку параметров ЭКС, ЭКГ, суточное мониторирование ЭКГ, УЗИ сердца и пробу с дозированной физической нагрузкой (при наличии показаний). Сроки наблюдения и объем обследования могут варьировать в зависимости от причин и особенностей течения синдрома.
Вакцинация: Вакцинация детей с СССУ проводится при отсутствии прогрессирования функции синусового узла. Прививки противопоказаны детям с аутоиммунными формами СССУ или постмиокардитического генеза в острой фазе заболевания. Если манифестация СССУ связана с ОРВИ или вакцинацией, прививки не проводятся. У пациентов с послеоперационным СССУ вакцинация возможна не ранее чем через 6 месяцев после коррекции врожденного порока сердца. Рекомендуется использовать инактивированные вакцины. Наличие ЭКС не является противопоказанием к вакцинации.
Занятия спортом: При асимптомной брадикардии с ЧСС ниже 5-го перцентиля относительно возрастных норм, паузах ритма до 2-2,5 секунд и адекватном приросте ЧСС на нагрузке без признаков миокардиальной дисфункции допускаются занятия всеми видами спорта.
Детям с структурными изменениями в сердце и имплантированным ЭКС занятия спортом разрешаются не ранее чем через 6 месяцев после операции, при условии нормального увеличения ЧСС на нагрузке, отсутствии аритмий и миокардиальной дисфункции. Контактные виды спорта исключаются. Разрешены виды спорта с низкими или средними динамическими и статическими нагрузками: боулинг, гольф, стрельба, автогонки, конный спорт, мотоспорт, гимнастика, парусный спорт, стрельба из лука, фехтование, настольный теннис, теннис (парный разряд), волейбол, легкая атлетика (прыжки, бег — спринт), фигурное катание (парное), синхронное плавание. При вариантах СССУ с ригидной брадикардией (ЧСС менее 40 уд/мин, паузы ритма более 2,5 секунд, миокардиальная дисфункция) занятия спортом не рекомендованы.
Пациенты могут иметь дополнительные ограничения, связанные с заболеваниями, ставшими причиной развития вторичного СССУ.
ПРОФИЛАКТИКА
Для своевременного выявления детей с пограничной брадикардией и группы риска по формированию синдрома, а также для ранней диагностики начальных стадий СССУ необходимо проводить ЭКГ-обследование. Если на стандартной ЭКГ выявляется брадикардия с частотой сердечных сокращений (ЧСС) ниже 5-го процентиля относительно возрастных норм, требуется осмотр кардиолога и контроль ЧСС один раз в год в течение не менее 5 лет. При брадикардии с ЧСС ниже 2-го процентиля также показан осмотр кардиолога, но контроль ЧСС следует проводить раз в 3 месяца.
Пациентам, которым показана имплантация электрокардиостимулятора (ЭКС), необходимо пройти психологическую реабилитацию до и после хирургического вмешательства.
Для профилактики постмиокардитических брадиаритмий важно предотвращать инфекционные заболевания у беременных и детей, а также своевременно назначать адекватную терапию при развитии инфекционного заболевания.
ИСХОДЫ И ПРОГНОЗ
Начальным этапом формирования синдрома слабости синусового узла (СССУ) является синусовая брадикардия.
Устойчивое снижение частоты сердечных сокращений (ЧСС) ниже 2-го перцентиля на стандартной ЭКГ, продолжительностью более 3 лет, связано с прогрессирующим нарушением функции синусового узла у детей. Раннее выявление пограничной брадикардии и адекватная оценка значений ЧСС могут предотвратить дальнейшее развитие дегенеративного процесса в проводящей системе сердца. Без лечения синдром может прогрессировать, проявляясь жалобами, изменениями на ЭКГ, ухудшением гемодинамики и нарушениями атриовентрикулярного и внутрижелудочкового проведения. Для прогноза заболевания у детей необходимо проводить комплексную оценку клинико-электрофизиологических показателей. В некоторых случаях клинические симптомы имеют большее значение, чем электрофизиологические данные. Принципы оценки эффективности лечения детей с СССУ отличаются от таковых при других нарушениях ритма. Стабильная клиническая и ЭКГ-картина при отсутствии положительной динамики может свидетельствовать о приостановлении патологического процесса.
Литература
-
Гордеев О.Л., Егоров Д.Ф., Лебедева В.К. и др. Возрастные нормативы электрофизиологических показателей функции синусового узла и атриовентрикулярного соединения у детей. // Вестник аритмологии, 2004, 35, приложение В: 224-228.
-
Комплексная диагностика синдрома слабости синусового узла. Методические рекомендации № 94/159 Министерства здравоохранения и медицинской промышленности РФ. // С-П., 1996, 45 с.
-
Кубергер М.Б. Руководство по клинической электрокардиографии детского возраста. // Ленинград: Медицина, 1983, 367 с.
-
Макаров Л.М. Холтеровское мониторирование. // М.: Медпрактика-М, 2003, 340 с.
-
Покровский В.М. Формирование ритма сердца в организме человека и животных. // Краснодар: Кубань-Книга, 2007, 143 с.
-
Полякова Е.Б. // Автореф. дис. канд. мед. наук М, 2007, 24 с.
-
Школьникова М.А. Жизнеугрожающие аритмии у детей. // М., 1999, 230 с.
-
Школьникова М.А., Миклашевич И.М., Калинин Л.А. (под ред.) Нормативные параметры ЭКГ у детей и подростков. // М., 2010, 231 с.
-
Allen H.D., Driscoll D.J., Shaddy R.E., Feltes T.F. Moss and Adams. Heart disease in infants, children, and adolescents: including the fetus and young adult. 7th ed. // Lippricont Williams&Wilkins, 2008. – Vol. 1. – 760 p.
-
Anderson J.B., Benson D.W. Genetics of sick sinus syndrome. // Card Electrophysiol Clin., 2010, 2(4):499-507.
-
Brignole M., Auriccio A., Baron-Esquivias G., Bordachar P. et al. Guidelines for cardiac pacing and cardiac resynchronization therapy. // Europace, 2013, 15:1070.
-
Brugada J., Blom N., Sarquella-Brugada G., Blomstrom-Lundqvist C. et al. Pharmacological and non-pharmacological therapy for arrhythmias in the pediatric population: EHRA and AEPC-Arrhythmia. // Europace, 2013, 15(9):1337-82.
-
Epstein A.E., DiMarco J.P., Ellenbogen K.A., Estes M.N.A., Freedman R.A. et al. 2012 ACCF/AHA/HRS Focused Update incorporated into the ACC/AHA/HRS 2008 Guidelines for device-based therapy of cardiac rhythm abnormalities. // Circulation, 2013, 127:e283-e352.
-
Kugler J. Sinus node dysfunction In Gilette P, Garsoan A (eds) Pediatric Arrhythmia Electrophysiology and pacing. // Philadelphia WB Saunders Co, 1990, 250-300.
-
Montague T.J, Taylor P.G, Stockton R., et al. The spectrum of cardiac rate and rhythm in normal newborns. // Pediatr Cardiol., 1982, 2:33-38.
-
Semelka M., Gera J., Usman S. Sick sinus syndrome: a review. // Am Fam Physician, 2013, 87(10):691-6.
-
Southall D.P, Johnston F, Shinebourne EA, et al. Twenty-four-hour electrocardiographic study of heart rate and rhythm patterns in a population of healthy children. // Br Heart J., 1981, 45:281-291.
-
Southall D.P, Richards J, Mitchell P, et al. Study of cardiac rhythm in healthy newborn infants. // Br Heart J., 1980, 43:14-20.
-
Zeigler V.L., Gillette P.G. Practical management of pediatric cardiac arrhythmias. // Futura Publishing Company, Inc. Armonk, NY, 2001. – 422 p.