У новорожденных гемофилия может проявляться длительным кровотечением из пуповины, подкожными гематомами и кефалогематомами. У детей первого года жизни кровотечения могут возникать при прорезывании зубов или после операций (например, инцизии уздечки языка, циркумцизии). Острые края молочных зубов могут травмировать язык, губы и щеки, вызывая кровотечения из слизистых оболочек. В грудном возрасте гемофилия встречается редко, так как материнское молоко содержит достаточное количество активной тромбокиназы.
Вероятность посттравматических кровотечений возрастает, когда ребенок начинает вставать и ходить. У детей старше года часто наблюдаются носовые кровотечения, подкожные и межмышечные гематомы, а также кровоизлияния в крупные суставы. Обострения геморрагического диатеза могут происходить после инфекций (ОРВИ, ветрянка, краснуха, корь, грипп) из-за нарушения проницаемости сосудов, что приводит к самопроизвольным геморрагиям. Постоянные и длительные кровотечения у детей с гемофилией могут вызывать анемию различной степени.
Частота кровоизлияний при гемофилии распределяется следующим образом: гемартрозы (70–80%), гематомы (10–20%), гематурия (14–20%), желудочно-кишечные кровотечения (8%), кровоизлияния в ЦНС (5%).
Гемартрозы — наиболее частое проявление гемофилии. Первые внутрисуставные кровоизлияния у детей с гемофилией возникают в возрасте 1–8 лет после травм или спонтанно. При гемартрозе наблюдаются выраженные боли, увеличение сустава, гиперемия и гипертермия кожи. Рецидивирующие гемартрозы могут привести к хроническому синовиту, деформирующему остеоартриту и контрактурам. Это, в свою очередь, нарушает динамику опорно-двигательного аппарата (искривление позвоночника и таза, гипотрофия мышц, остеопороз, вальгусная деформация стопы) и может привести к инвалидности в детском возрасте.
Кровоизлияния в мягкие ткани, такие как подкожная клетчатка и мышцы, также часто встречаются при гемофилии. У детей могут наблюдаться непроходящие синяки на туловище и конечностях, а также глубокие межмышечные гематомы, склонные к распространению. Обширные гематомы могут сдавливать крупные артерии и нервы, вызывая сильные боли, паралич, атрофию мышц или гангрену.
Кровотечения из десен, носа, почек и органов ЖКТ также распространены. Они могут быть вызваны медицинскими манипуляциями (внутримышечными инъекциями, экстракцией зуба, тонзиллэктомией и др.). Особенно опасны кровотечения из зева и носоглотки, так как они могут привести к обструкции дыхательных путей и потребовать экстренной трахеостомии. Кровоизлияния в мозговые оболочки и головной мозг могут вызвать тяжелые поражения ЦНС или летальный исход.
Гематурия может возникать самопроизвольно или из-за травм поясничной области, сопровождаясь дизурическими явлениями и приступами почечной колики при образовании сгустков в мочевыводящих путях. У больных с гемофилией часто выявляются пиелоэктазия, гидронефроз и пиелонефрит.
Желудочно-кишечные кровотечения могут быть связаны с приемом НПВС и другими лекарствами, обострением язвенной болезни, эрозивным гастритом или геморроем. Кровоизлияния в брыжейку и сальник могут имитировать острый живот, требуя дифференциальной диагностики с острым аппендицитом и кишечной непроходимостью.
Характерным признаком гемофилии является отсроченное кровотечение, которое обычно возникает не сразу после травмы, а через 6–12 часов и более.
Патогенез и лабораторная диагностика. Существует два вида гемостаза — сосудисто-тромбоцитарный (первичный) и коагуляционный. Ферментный каскад коагуляционного гемостаза имеет внутренний (контактный) и внешний пути активации. Оба пути замыкаются на образовании протромбиназного комплекса, состоящего из Х (Стюарта-Прауэра) и V (проакцелерина) факторов, ионов кальция и фосфолипидных матриц. Запуск внешнего пути инициируется тканевым тромбопластином (фактор II), поступающим в кровь. В лабораторной диагностике данный путь оценивается с помощью протромбинового (тромбопластинового) теста.
Факторы VIII и IX участвуют только во внутренней активации гемостаза. Фактор VIII (антигемофильный глобулин) и фактор IX (Кристмаса) в комплексе с ионами кальция и фосфолипидами активируют фактор X и формируют протромбиназный комплекс. Это объясняет особенности коагулограммы при гемофилии: нормальные протромбиновый показатель и тромбиновое время при удлиненном времени свертывания цельной крови, кальцифицированной цитратной плазмы и активированного частичного тромбопластинового времени (АЧТВ).
Количество фактора VIII в крови, как и других факторов свертываемости, измеряется в процентах. За основу берется среднее количество фактора в популяции, выраженное в «единицах (ед.) на 1 мл» или «100 ед. на децилитр (100 U/dl)». Таким образом, 100% — это не максимальное значение, а среднее. Нормальный уровень фактора VIII составляет 50-180%. В зависимости от этого уровня гемофилия типа А делится на тяжелую (менее 1%), средней тяжести (1-5%) и легкую (более 5%).
Измерение активности фактора VIII (VIII:C) является специфичным признаком гемофилии типа А, но не единственным. У больных этим заболеванием уровень фактора ниже 25%. При более высокой активности фактора VIII кровотечения даже при травмах нехарактерны. Уровень 25-50% наблюдается у 1/3 носителей аномального гена. Уровень 50-180% является средним для популяции, а более высокий встречается у беременных. Носительство аномальных генов может проявляться повышенной склонностью к кровотечениям, особенно после экстракции зуба и меноррагий.
Для диагностики гемофилии и подобных расстройств необходимо провести тесты гемостаза: протромбиновое время, АЧТВ, время кровотечения и количество тромбоцитов. При гемофилии повышается только АЧТВ. Важно помнить, что при легком течении болезни лабораторные показатели могут быть нормальными, особенно в стрессовых ситуациях (операции, травмы), так как еще в 1772 году было отмечено, что кровь, взятая после стресса, свертывается быстрее.
Наиболее достоверным методом диагностики гемофилии и ее носительства является молекулярно-генетическое исследование. Методика выявления полиморфизма ДНК (RFLP — полиморфизм длины ограниченного фрагмента, VNTR — непостоянное число тандемных дупликаций) позволяет диагностировать нарушения генов факторов свертывания с достоверностью более 99%. Ее можно использовать в пренатальной диагностике, исследуя ДНК, экстрагированную из клеток ворсин хориона на 10-й неделе беременности или позже. Еще более достоверна методика полимеразной цепной реакции, позволяющая выявлять конкретные изменения в хромосомах: делеции, инверсии и т. д.
Клинико-анатомическая картина. Главным и практически единственным признаком гемофилии является склонность к кровотечениям. У лиц с тяжелой формой заболевания часты спонтанные кровотечения, а тесты свертываемости крови всегда выявляют патологию. При среднетяжелой форме возможны спонтанные кровотечения после незначительных травм, АЧТВ всегда увеличено. Легкая форма проявляется склонностью к кровоточивости после травм и операций, спонтанных кровотечений не бывает, тесты свертываемости крови могут быть в пределах нормы. При легкой форме заболевания диагноз часто ставится впервые в уже зрелом возрасте.
При тяжелом и среднетяжелом течении гемофилии, когда гемартрозы становятся частыми и обильными, синовиальная оболочка не может полностью реабсорбировать кровь из полости сустава и гипертрофируется. Это нарушает функцию сустава, снижает его подвижность и приводит к хроническому синовиту. Выделяют острую и подострую формы гемартрозов.
Любая травма у больного гемофилией может вызвать даже незначительное, но непрекращающееся кровотечение. Поэтому внутримышечные инъекции запрещены. Иммунизацию и введение лекарств лучше проводить подкожно, используя тонкие иглы и обеспечивая 5-минутное давление на место инъекции. Часто наблюдаются носовые кровотечения и кровотечения из ротовой полости (например, при прикусывании языка или травме десен). Наиболее опасны внутренние кровотечения и кровоизлияния в полость черепа. Упорная гематурия и наличие крови в кале также возможны. Даже незначительное, но длительное выделение крови приводит к анемии. Кровоизлияния в забрюшинную клетчатку и полость черепа представляют опасность для жизни.
Гемофилия характеризуется частыми рецидивирующими кровопотерями, что приводит к анемизации больных. Как и в общей популяции, основными причинами смерти пациентов с гемофилией являются онкологические и сердечно-сосудистые заболевания. Однако у больных гемофилией часто причиной смерти становятся травматические кровоизлияния в полость черепа, а также ВИЧ-инфекция и поражение печени вирусом гепатита С, связанные с частыми гемотрансфузиями.
Среди осложнений гемофилии выделяют суставной геморрагический синдром (контрактуры, переломы, артропатия), кровоизлияния в мягкие ткани (опухолевидные образования, инфицирование), заражение трансмиссивными агентами (вирусы гепатитов А, В, С, ВИЧ, парвовирус В19, болезнь Крейтцфельдта-Якоба и др.), а также формирование ингибиторов (антител) к факторам свертывания, что резко снижает эффективность лечения.
СХЕМА НАСЛЕДОВАНИЯ ГЕМОФИЛИИ
ВЫЯВЛЕНИЕ НОСИТЕЛЯ ГЕМОФИЛИИ
Носителей гемофилии можно условно разделить на две группы: «облигатные» и «возможные». К «облигатным» относятся женщины, у которых отец болен гемофилией или есть два и более сына с этим заболеванием, а также женщины с одним больным сыном и родственником-мужчиной по линии матери, страдающим гемофилией. К «возможным» носителям относятся женщины с одним или более родственниками, страдающими гемофилией по линии матери, но у которых сыновья здоровы, а также те, у кого гемофилией болен только один сын.
Большинство носителей гемофилии не имеют симптомов, однако некоторые женщины с низким уровнем активности факторов F VIII и F IX могут легко образовывать кровоподтеки, испытывать чрезмерное кровотечение после операций или удаления зубов, а также проявлять другие признаки, включая меноррагию.
Уровень активности факторов свертываемости крови у носителей гемофилии близок к норме, поэтому выявление носителя только по анализу крови невозможно.
Первым шагом в определении, является ли женщина носителем гемофилии А или В, должно стать составление подробного семейного древа. Отношение женщины-носителя к мужчине, страдающему гемофилией, определяется через ее связь с матерью и родственницами. Следующий шаг — определение уровня активности фактора свертываемости F VIII и антигена фактора фон Виллебранд для возможного носительства гемофилии А, и уровня активности фактора F IX для гемофилии В. Рекомендуется проводить анализ крови не менее трех раз из-за естественной вариативности.
Этот анализ позволяет в 80% случаев выявить носителя гемофилии А и в 50% случаев — носителя гемофилии В.
Если уровень активности факторов F VIII и F IX нормальный, это не является доказательством отсутствия гена гемофилии.
Третий и наиболее точный шаг в выявлении носителя гемофилии — анализ ДНК, который также важен при пренатальной диагностике.
ИСПОЛЬЗОВАНИЕ МЕТОДА ПОЛИМОРФИЗМА В ДИАГНОСТИКЕ
При выявлении носителя гемофилии методом анализа ДНК и в пренатальной диагностике используется методика изучения полиморфизма ДНК, как внутри гена F VIII или F IX, так и в его близости. Полиморфизмы (например, RFLP или VNTR) позволяют при использовании интрагенного полиморфизма в 95% случаев получить информативные результаты с вероятностью более 99%. При использовании экстрагенной методики степень достоверности снижается до 95%. Эта информация важна для пренатальной диагностики. На десятой неделе беременности или позже можно экстрагировать ДНК плода из ворсин хориона для анализа на наличие соответствующего полиморфного маркера, выявленного у матери. Выявление носителя гемофилии требует анализа ДНК ближайших родственников, включая больного гемофилией и родителей предполагаемого носителя. Для полноты анализа желательно привлечь как можно больше родственников.
ВЫЯВЛЕНИЕ СПЕЦИФИЧНЫХ НАРУШЕНИЙ ГЕНА
Специфические нарушения гена все чаще идентифицируются с помощью технологий, основанных на усилении последовательностей ДНК с помощью Южного метода или полимерной цепочной реакции (PCR). Эти методы применяются только в специализированных центрах и требуют высокой квалификации персонала. Дальнейшие разработки в этой области могут значительно упростить процедуры, делая их более доступными для рутинного генетического исследования. Одним из важных достижений является идентификация инверсии в части Х-хромосомы, которая вызывает разделение гена F VIII на две части и нарушает его нормальное функционирование.
ПРЕИМУЩЕСТВА АНАЛИЗА ДНК
Для выявления повреждений гена и полиморфизма требуется образец ДНК, обычно извлекаемый из образца крови (необходимы белые кровяные тельца). Преимущество анализа ДНК перед анализом активности факторов свертываемости крови заключается в его большей точности при выявлении статуса носителя гемофилии и в пренатальной диагностике. ДНК стабильна в замороженном состоянии, что позволяет легко транспортировать образцы крови и анализировать их даже после длительного хранения. Важно собирать как можно больше образцов крови больных гемофилией и их родственников для будущих научных исследований. Рекомендации Всемирной федерации гемофилии по сбору и хранению образцов ДНК можно найти в приложении к изданию.
СТЕПЕНЬ ТЯЖЕСТИ ЗАБОЛЕВАНИЯ ГЕМОФИЛИЕЙ
Клиническая картина гемофилии варьируется от семьи к семье, однако в пределах одной семьи уровень активности факторов свертываемости крови F VIII или F IX обычно одинаков. Нормальный уровень активности фактора составляет 50-150%, но у пациентов с показателем 30% редко возникают значительные кровотечения, и заболевание может быть выявлено только при серьезной операции или травме.
Таблица 1. Классификация типов гемофилии
| % факторов F VIII или F IX | Степень проявления гемофилии | Основные характеристики |
|---|---|---|
| 1% или менее (> 0,01 ед-ц/мл) | Тяжелая | Частые спонтанные кровотечения. Тесты на свертываемость крови всегда выявляют патологию |
| >1-5% (>0,01 — 0,05 ед-ц/мл) | Средняя | Отдельные спонтанные кровотечения. Кровотечения после небольших травм. Длительное частичное время тромбопластина |
| >5-30% (0,05 — 0,3 ед-ц/мл) | Легкая | Кровотечения возникают только после травмы или операции. Тесты на свертываемость крови могут быть в пределах нормы |
| 30-50% (0,3 — 0,5 ед-ц/мл) | Очень легкая | Аномальные кровотечения могут проявляться или нет после операции или травмы. Тесты на свертываемость крови обычно в норме |
Длительные или повторяющиеся кровотечения могут возникать в одном или нескольких местах после незначительной травмы, что делает их спонтанными. Кровотечения, как правило, внутренние, что приводит к гемартрозам, гематомам в мышечной ткани или других органах, а также к кровоизлияниям в области ЦНС.
Таблица 2. Возможные места кровоизлияний
| Тип кровоизлияния | Частотность случаев (%) |
|---|---|
| Гемартрозы | 70 — 80 |
| Гематомы в подкожных и мышечных тканях | 10 — 20 |
| Другие виды часто случающихся кровотечений | 5 — 10 |
| Кровотечения в области ЦНС | < 5 |
Таблица 3. Распространенность кровоизлияний в зависимости от сустава
| Место гемартроза | Частотность случаев (%) |
|---|---|
| Колено | 45 |
| Локоть | 30 |
| Голеностопный сустав | 15 |
| Запястье | 3 |
| Плечо | 3 |
| Бедро | 2 |
| Другое | 2 |
Частота кровотечений может проявляться у детей в раннем возрасте, например, после обрезания. Часто образуются синяки с припухлостью. Интенсивность их образования может вызвать подозрения о насилии. Заметные опухоли и нежелание ребенка пользоваться конечностями могут свидетельствовать о кровоизлиянии в мышечную ткань или сустав. Кровотечения изо рта или языка также распространены в этом возрасте и связаны с падениями.
Повторные кровотечения в суставах, которые не лечатся или лечатся неадекватно, могут привести к инвалидности из-за поражения синовиальной оболочки и суставных поверхностей. Эти нарушения могут вызвать гипотрофию мышц, что, в свою очередь, становится причиной повторных кровотечений. Если в суставе происходят повторные кровотечения, его называют «суставом-мишенью».
Также возможны кровотечения из носа, желудка, ротовой полости и гематурия, которые могут быть продолжительными. В таких случаях необходимо исключить местные причины. В прошлом интракраниальные кровотечения часто приводили к летальному исходу, но их частота снизилась благодаря ранней терапии травм головы. Кровоизлияния в области шеи и забрюшинной клетчатки также представляют угрозу для жизни.
Кровотечения могут происходить из-за травмы, хирургического вмешательства, удаления зубов или внутримышечных инъекций. Иммунизацию лучше проводить подкожно, принимая меры предосторожности, используя тонкие иглы и обеспечивая местное давление в течение пяти минут после инъекции.
Гемофилия средней тяжести (> 1 — 5 %)
Интенсивность кровотечений такая же, как при тяжелой форме гемофилии, но частота значительно ниже и связана с травмами. При средней тяжести гемофилии уменьшается вероятность инвалидности. Интенсивные кровотечения могут возникать после всех форм хирургического вмешательства и удаления зубов. Лекарства рекомендуется вводить перорально, ректально или внутривенно, но не внутримышечно.
Слабая форма гемофилии (>5 — 30 %)
Многие люди с легкой формой гемофилии узнают о диагнозе позже, когда после операции, удаления зуба или травмы начинается сильное кровотечение. У таких людей также могут быть кровоизлияния в мышечные ткани или суставы после значительных травм.
Детей с гемофилией следует поощрять вести обычный образ жизни, однако они и их родители должны знать о потенциальных последствиях травм.
ДИАГНОСТИКА
Первым шагом в диагностике является сбор подробной истории пациента и его семьи, включая вопросы о склонности к образованию кровоподтеков, кровотечениям после обрезания, удаления зубов или тонзиллэктомии, а также о частоте кровотечений у близких родственников. У любого человека с продолжительными или необъяснимыми кровотечениями необходимо подозревать гемофилию и проводить соответствующие тесты.
Вторым шагом является тест на гемостаз: продолжительность кровотечения по времени АРРТ, время протромбина (РТ). Время кровотечения обычно «в норме», так как функции тромбоцитов при гемофилии не нарушены. Если уровень факторов свертываемости крови менее 30%, этап АРРТ необходимо продлить. У некоторых больных с легкой формой гемофилии результаты скринингового теста могут быть нормальными. Если АРРТ выявляет аномалии или в истории семьи отмечены нарушения крови, необходимо провести анализ уровня активности факторов свертываемости крови, для чего пациента могут направить в специализированный центр. Следует помнить, что диагноз легкой формы гемофилии может быть затруднен, если человек перенес операцию, так как уровень F VIII может повышаться в ответ на стресс, и факторный анализ следует повторить позже.
При первоначальном обследовании и дальнейших консультациях необходимо брать образцы крови для анализа на наличие ингибиторов факторов свертываемости крови, вирусов гепатита и ВИЧ. У больных гемофилией А слабой и средней формы (дефицит фактора F VIII) необходимо проверить реакцию на применение DDAVP (десмопрессин), так как этот препарат может избежать применения продуктов крови.
Что необходимо учитывать при кровотечениях. Больной тяжелой формой гемофилии обычно может определить наличие кровотечения по характеру боли. Часто пациент ощущает боль до появления припухлости или других симптомов. Врач и медсестра должны быть внимательны к жалобам пациента и начинать терапию немедленно, не дожидаясь видимых симптомов. Кровотечение может проявиться в любое время без заметных причин, и лечение следует начинать как можно быстрее при:
- кровотечении в суставе
- кровотечении в мышце (отсроченное лечение может привести к сдавливанию сосудов и нервов)
- ранах в области шеи, рта, языка, лица и глаза (длительные кровотечения могут перекрыть доступ воздуха)
- ударах по голове и необычной головной боли (в 30% случаев интракраниальных кровотечений не отмечается травм в истории)
- обильных и продолжительных кровотечениях в любой области
- сильной боли или заметной опухоли в любой области (кровотечение может указывать на другие патологии, например, кровоизлияния в подвздошной области могут свидетельствовать об остром аппендиците)
- открытых ранах, требующих наложения швов (необходима повторная терапия до заживления раны)
- любых несчастных случаях, которые могут привести к кровотечениям (для профилактики требуется меньший расход препаратов крови, чем при уже начавшемся кровотечении).
ЛЕЧЕНИЕ
Лечение в большинстве случаев заключается в переливании препарата, содержащего недостающий фактор, для повышения его уровня в крови. Дополнительные меры могут включать покой, холод, наложение шины, местное или системное применение антифибринолитических препаратов, а также физиотерапию до полного выздоровления. Дополнительные дозы продуктов крови могут быть необходимы для восстановления подвижности при кровотечениях в суставе и мышцах, чтобы реабилитация проходила успешно без дополнительных кровоизлияний и снижалась вероятность долгосрочных осложнений, таких как хронический синовит, артрит, образование кисты костной ткани и контрактуры.
Для лечения гемофилии А можно использовать свежую или замороженную плазму. Открытие в 1964 году криопреципитата, богатого фактором F VIII, обеспечило возможность достижения удовлетворительного гемостатического уровня F VIII и стало стартом для создания многих концентратов факторов свертываемости крови.
При легкой форме гемофилии первым средством лечения должен стать DDAVP (аналог вазопрессина, который освобождает факторы F VIII и фон Виллебранда из мест хранения в организме). Препарат вводится внутривенно, подкожно или интраназально в виде спрея. DDAVP может использоваться для лечения кровотечений после травм и для повышения уровня фактора в крови перед удалением зубов и операциями. Он бесполезен при тяжелой форме гемофилии и ограничен при средней тяжести.
Заместительная терапия фактором при гемофилии В может осуществляться свежей или замороженной плазмой, однако невозможность использования необходимых объемов вещества затрудняет достижение удовлетворительного уровня фактора в крови.
Разработка методов лечения гемофилии А и В привела к созданию концентратов факторов F VIII и F IX. Первые концентраты F IX известны как концентраты протромбинового комплекса (РСС), так как содержат другие факторы свертываемости крови, зависимые от витамина К (FII, FVII, FX). Концентраты РСС известны как тромбогенные, особенно при лечении пациентов, иммобилизованных после обширной операции. Позже были разработаны чистые концентраты фактора F IX.
ДОЗИРОВКА
Адекватная дозировка зависит от объема плазмы, уровня фактора в крови на момент лечения, активности препарата и степени восстановления его активности. Доза должна обеспечивать незамедлительное действие, как по мнению врача, так и по ощущениям пациента. Таким образом, дозировка будет варьироваться от пациента к пациенту и зависеть от состояния сустава и степени тяжести кровоизлияния. Дозы ниже рекомендуемых могут быть эффективны только при раннем применении.
Таблица 4. Достаточный гемостатический уровень F VIII и F IX в различных клинических ситуациях и дозировка концентратов F VIII и F IX.
| Клиническая ситуация | Необходимая концентрация плазмы % от плазмы, полученной из пула | Необходимая для гемостаза доза МЕ на кг веса тела |
|---|---|---|
| Гемартроз и незначительные гематомы | 15-25 | 10-15 |
| Тяжелые гемартрозы и значительные гематомы | 30-60 | 20-35 |
| Хирургическое вмешательство и кровотечения, угрожающие жизни | 60-100 | 40-60 |
Повторное введение рекомендуемых доз может потребоваться в течение нескольких дней после значительной травмы или операции, а также после рассасывания обширной гематомы в мышечной ткани.
Лечение может понадобиться для восстановления подвижности после кровотечений в суставе или мышце, чтобы реабилитация проходила без повторных кровоизлияний.
Профилактическая терапия, проводимая регулярно для предотвращения кровотечений, используется в некоторых странах, особенно для детей и подростков. Краткосрочная профилактика на основе регулярного введения препаратов, например, три раза в неделю в течение нескольких недель, часто применяется для предотвращения повторного кровотечения в «сустав-мишень». Разовая профилактика может быть полезна перед стрессовыми событиями, такими как экзамены, путешествия или тренировки с необычной нагрузкой.
Антифибринолитические препараты, предотвращающие разрушение сгустков крови, могут быть эффективным дополнением к заместительной терапии после удаления зубов, при открытых ранах и меноррагии. Основной побочный эффект — тошнота. Наиболее известные препараты — Amicar (эпсилоновая аминокапроновая кислота) и Циклокапрон (транэкзаминовая кислота). Эти препараты не следует использовать одновременно с РСС, так как это повышает риск тромбоэмболии.
Аспирин и аспириносодержащие препараты необходимо избегать, так как они негативно влияют на тромбоциты. Другие препараты с побочными эффектами на тромбоциты также следует использовать с осторожностью. Для лечения хронической боли можно применять нестероидные противовоспалительные препараты (NSAIA), но только после еды, и их следует прекращать при появлении дискомфорта в эпигастральной области или кровотечений в желудочно-кишечном тракте.
Адекватное лечение позволяет даже больным с тяжелой формой гемофилии вести полноценную жизнь и быть активными членами общества.
ОСЛОЖНЕНИЯ ПРИ ЛЕЧЕНИИ
Основные осложнения при лечении гемофилии связаны с заражением вирусами, содержащимися в крови, и появлением ингибиторов.
- Гепатит
- ВИЧ-инфекция и СПИД
- Толерантность к F VIII
- Тромбоз
- Аллергическая реакция
- Гемолиз
ПРОФИЛАКТИКА ГЕМОФИЛИИ
Избежать рождения ребенка с гемофилией возможно только при достоверном выявлении носителей заболевания и консультациях по вопросам пренатальной диагностики. Раннее обращение за консультацией по вопросам материнства или прерывания беременности поможет избежать эмоциональных травм. Рекомендуется проводить генетические исследования среди всех членов семьи сразу после диагностики гемофилии у одного из них. Предпочтительно сообщать детям о статусе носителя гемофилии в возрасте, когда они могут это осознать, обычно в 12 лет, хотя иногда информация может быть предоставлена и раньше, если уровень активности факторов F VIII или F IX низок и требуется регулярное лечение.
Важно помнить, что в процессе анализа не только выявляется носитель гемофилии, но и может быть получен результат о том, что испытуемый не является таковым.
Консультирование по вопросу о носителе гемофилии должно проводиться так, чтобы женщина не испытывала чувства вины за свой выбор. При обсуждении генетических аспектов важно учитывать мнение самих больных гемофилией. Идеально, если генетическое консультирование проводят специалисты, обладающие знаниями о гемофилии, однако во многих странах эту работу выполняет медицинский персонал. Специалист должен помнить, что ни один тест не является окончательно достоверным, и носителю гемофилии можно сообщать лишь о вероятности риска, а не о точном диагнозе.
Выбор для носителей гемофилии и их партнеров может включать решение не иметь детей или усыновить, провести преимплантационную диагностику при оплодотворении «ин витро», или пренатальную диагностику, включая возможность рождения сына с гемофилией или дочери-носителя. При выборе диагностики на 10 неделе беременности или позже будет проведен генетический анализ хориальных ворсин, на 14-15 неделе — пункция плодного пузыря для определения пола плода, а на 18 неделе — анализ крови плода для определения уровня факторов свертываемости крови. Эти тесты должны проводиться в специализированных учреждениях.
Даже при эффективном планировании семьи рождение детей с гемофилией невозможно полностью предсказать, так как 20-30% случаев относятся к семьям, не зарегистрированным в группе риска, и могут быть результатом новых мутаций.
ЗАКЛЮЧЕНИЕ
Гемофилия — наследственное заболевание, требующее медицинского контроля на протяжении всей жизни пациента. Лечение направлено на снижение риска инвалидности, продление жизни, создание условий для социального и физического благосостояния больных и помощь в раскрытии их жизненного потенциала. Ключевым аспектом лечения гемофилии является адекватная поставка безопасных и эффективных препаратов, которые должны вводиться на самых ранних стадиях кровоизлияний.
За последние 30 лет достигнуты значительные успехи в организации лечения гемофилии благодаря новым технологиям производства препаратов и принципу комплексной помощи. ВИЧ-инфекция продолжает оказывать влияние на сообщество людей с гемофилией, особенно в развитых странах, однако постоянная работа над улучшением очистки препаратов крови делает их все более безопасными. Достижения молекулярной биологии и технологии рекомбинантной ДНК позволили разработать синтетические концентраты факторов свертываемости крови, проводить более точное выявление носителей заболевания и пренатальную диагностику, а также дают надежду на то, что в будущем генная терапия решит проблему гемофилии.
Солидная родословная
Генная мутация, вызывающая гемофилию, является случайным событием. Большинство вредных мутаций отбрасываются естественным отбором: их носители не доживают до половой зрелости. Однако некоторые генетические изменения закрепляются в популяции, как произошло с гемофилией.
Случаи повышенной кровоточивости известны с древних времен. Люди быстро поняли, что это наследственное заболевание, наблюдая за целыми поколениями семей. Однако для выяснения причин гемофилии потребовались десятилетия.
Гемофилия получила название «викторианской» или «царской» болезни, когда проявилась в семье английских монархов. Носительницей мутантного гена оказалась королева Виктория, которая передала его своим дочерям и сыну. Ее внучка, принцесса Алиса-Виктория-Елена-Луиза-Беатрис Гессен-Дармштадтская, в крещении Александра Федоровна, вышла замуж за русского императора Николая II и передала ген гемофилии своему сыну Алексею.
Наследование гемофилии…
Гемофилия — рецессивное заболевание, связанное с полом. Если в половых хромосомах присутствует ген гемофилии, мальчик рождается больным, а девочка становится носителем и может передавать этот ген своим детям.
Мужчина с гемофилией будет иметь здоровых сыновей, но все его дочери станут носительницами мутации.
Носительница гемофилии обычно не проявляет симптомов, но с вероятностью 50% передает ген своим детям: 25% — шанс рождения девочки-носительницы и 25% — мальчика с гемофилией.
Случаи гемофилии у женщин также возможны, если отец болен гемофилией, а мать — носительница мутантного гена.
В 20–30% случаев болезнь может возникнуть из-за случайной мутации в половых клетках, когда оба родителя здоровы и не имеют генов гемофилии.
…и ее причины
Гемофилия возникает из-за отсутствия белков, отвечающих за свертывание крови. В организме человека насчитывается 13 факторов свертывания в плазме и 22 в тромбоцитах.
Мутация в X-хромосоме приводит к дефициту фактора VIII (гемофилия А) или фактора IX (гемофилия В). Эти белки, которые образуются в печени, имеют сложную структуру. У пациентов с гемофилией их уровень в крови значительно снижен или факторы отсутствуют. Тяжесть заболевания зависит от концентрации факторов свертываемости.
Диагностика гемофилии
У мальчиков с врожденной патологией гемофилия обычно проявляется в первый год жизни. Иногда симптомы появляются позже, когда ребенок начинает активно передвигаться и получает первые синяки и шишки.
У таких детей время остановки кровотечения значительно увеличивается. Подкожные гематомы могут достигать больших размеров и медленно рассасываться. Часто наблюдаются кровотечения в коленных и голеностопных суставах. Ребенок выглядит хрупким, с бледной кожей, слабым и болезненным.
Для подтверждения диагноза проводят коагулограмму. Обращают внимание на замедление активированного частичного тромбопластинового времени (АЧТВ) и определяют уровень факторов свертываемости крови VIII и IX в процентах от нормы. На основе этих данных оценивают тяжесть заболевания и выбирают тактику лечения.
Лечение гемофилии в прошлом…
Ранее врачи использовали различные средства для лечения кровоточивости, включая экстракты яичного белка, змеиный яд и арахисовую муку.
В 1840 году для лечения гемофилии начали применять донорскую кровь, но нехватка знаний о групповой совместимости и риск инфекционных осложнений ограничили распространение этого метода.
В начале 50-х годов XX века медики освоили переливание плазмы крови, что стало значительным шагом в лечении болезни. Однако пациенты оставались привязанными к больнице, так как первая помощь при травмах могла оказываться только квалифицированным персоналом.
Прорыв в лечении гемофилии произошел в 1965 году. Доктор Джудит Грэхем Пул, медленно размораживая плазму для переливания, обнаружила темный осадок — криопреципитат, который успешно использовали для остановки кровотечений. Этот осадок содержал концентрированные факторы свертываемости крови.
Вскоре концентрат начали производить промышленно и упаковывать в небольшие контейнеры для хранения в домашних холодильниках. Эти препараты до сих пор применяются для лечения гемофилии.
С внедрением препаратов крови возникла новая проблема — массовое распространение вирусов СПИДа, гепатитов А, В, С и других опасных заболеваний. Для борьбы с ними стали использовать различные методы обеззараживания крови, которые, к сожалению, не обеспечивают стопроцентную безопасность.
…и в настоящем
Сегодня основным методом лечения гемофилии остается заместительная терапия факторами крови. Существует множество препаратов, но все они имеют высокую стоимость. В России предусмотрено бесплатное обеспечение больных гемофилией препаратами факторов крови и другими лекарствами. Финансирование осуществляется из федерального бюджета и средств субъектов РФ.
Предпочтение отдается рекомбинантным факторам свертываемости. Эти препараты не содержат болезнетворных вирусов, но отличаются высокой ценой. Их синтезируют бактерии, в геном которых внедрен участок ДНК человека, отвечающий за образование необходимого фактора.
Широко используются лиофилизированные концентраты факторов VIII и IX, изготовленные из донорской крови и прошедшие многоступенчатую очистку от ВИЧ и вирусов гепатита. Эти препараты пациенты могут вводить самостоятельно после растворения, что минимизирует риск инфекционного заражения.
При отсутствии рекомбинантных и человеческих факторов продолжают использовать криопреципитаты и нативную донорскую плазму. В качестве дополнительного лечения применяются средства, стимулирующие свертываемость крови, и десмопрессин для легкой формы гемофилии.
Наиболее эффективной является схема профилактического введения факторов свертываемости. Больным необходимо вводить их внутривенно несколько раз в неделю на протяжении всей жизни.
ГМО против гемофилии
Перспективные разработки ведут ученые-генетики. Методы генной инженерии могут радикально излечить болезни, а не просто устранять их симптомы. Введение гена, отвечающего за синтез факторов свертываемости крови, может навсегда избавить человека от гемофилии.
С помощью генной инженерии уже удалось победить гемофилию у мышей. Ученые ввели человеческий фрагмент ДНК, отвечающий за выработку факторов свертываемости крови, в вирусный геном. Затем они заразили печень больных мышей этими модифицированными вирусами. Попав в клетки, вирусы внедрили свою ДНК с человеческим фрагментом в ДНК гепатоцитов, что привело к нормальному синтезу факторов свертываемости крови. Мыши, участвовавшие в эксперименте, выздоровели.
Пренатальная диагностика гемофилии
В 2/3 случаев гемофилия у детей передается от родителей и бабушек с дедушками. Современные методы пренатальной диагностики позволяют с вероятностью 95% (для европеоидной расы) предсказать наличие болезни у ребенка на сроке 11–12 недель.
Если будущий отец болен гемофилией или мать является носительницей (если среди родственников были гемофилики), необходимо провести биопсию ворсин хориона на сроке 10–11 недель. В 12–15 недель можно выполнить амниоцентез, а на сроке 18–22 недели — кордоцентез. Эти методы обеспечивают высокую точность диагностики гемофилии у плода. В случае положительного результата, даже если пара решает сохранить ребенка, результаты обследования важны для планирования родов и послеродового ухода.
Автор: Наталья Долгополова, врач-терапевт
В материале использованы фотографии, принадлежащие shutterstock.com
Источник: www.medweb.ru
При доминантном Х-сцепленном наследовании болезнь чаще встречается у женщин, так как они могут получить патологический аллель от обоих родителей. Мужчины наследуют этот ген только от матери. Женщины передают патологический признак как дочерям, так и сыновьям. Мужчина с доминантным мутантным геном передает его всем дочерям, но сыновья остаются здоровыми, так как получают Y-хромосому от отца. В среднем женщины болеют менее тяжело, чем мужчины, и клиническое течение болезни более вариабельно у гетерозиготных женщин.
По Х-сцепленному доминантному типу наследуется D-резистентный рахит (наследственная гипофосфатемия). При некоторых заболеваниях мужчины-гемизиготы могут погибать на ранних стадиях онтогенеза (синдром недержания пигмента, синдром Гольца-Горлина, рото-лице-пальцевой синдром). В таких случаях в родословных среди пораженных будут только женщины, и соотношение больных дочерей, здоровых дочерей и здоровых сыновей составит 1:1:1.
При Х-сцепленном рецессивном наследовании болезнь проявляется преимущественно у гемизиготных мужчин. Женщины, как правило, являются гетерозиготами и фенотипически здоровы, но могут быть носительницами. Болезнь у женщин проявляется только в гомозиготном состоянии, что вероятно при близкородственных браках. Чаще встречаются фенотипически здоровые родители, где мать является гетерозиготным носителем мутантного гена. В таких семьях болезнь передается половине сыновей, а дочери остаются здоровыми, но половина из них может быть гетерозиготными носителями. К Х-сцепленным рецессивным болезням относятся гемофилия, мышечная дистрофия Дюшена-Беккера, дальтонизм, синдром Хантера.
Y-сцепленное наследование связано с наличием Y-хромосомы только у мужчин. Гены, локализованные в Y-хромосоме, действуют только у мужчин и передаются по мужской линии от отца к сыну. По этому типу наследуется гипертрихоз ушной раковины. В Y-хромосоме также находятся гены, отвечающие за развитие семенников, сперматогенез (фактор азооспермии) и контроль роста тела, конечностей и зубов.
6. В последнее время выделяется митохондриальный тип наследования. Митохондрии передаются с цитоплазмой яйцеклеток, так как спермии не содержат митохондрий. В яйцеклетке находится около 25,000 митохондрий, каждая из которых содержит кольцевую хромосому. Генные мутации в митохондриальной ДНК связаны с атрофией зрительного нерва Лебера, митохондриальными миопатиями и прогрессирующими офтальмоплегиями. Болезни, обусловленные этим типом наследственности, передаются от матери как дочерям, так и сыновьям в равной степени. Больные отцы не передают болезни ни дочерям, ни сыновьям.
Источник: helpiks.org
Краткая физиология свертываемости крови
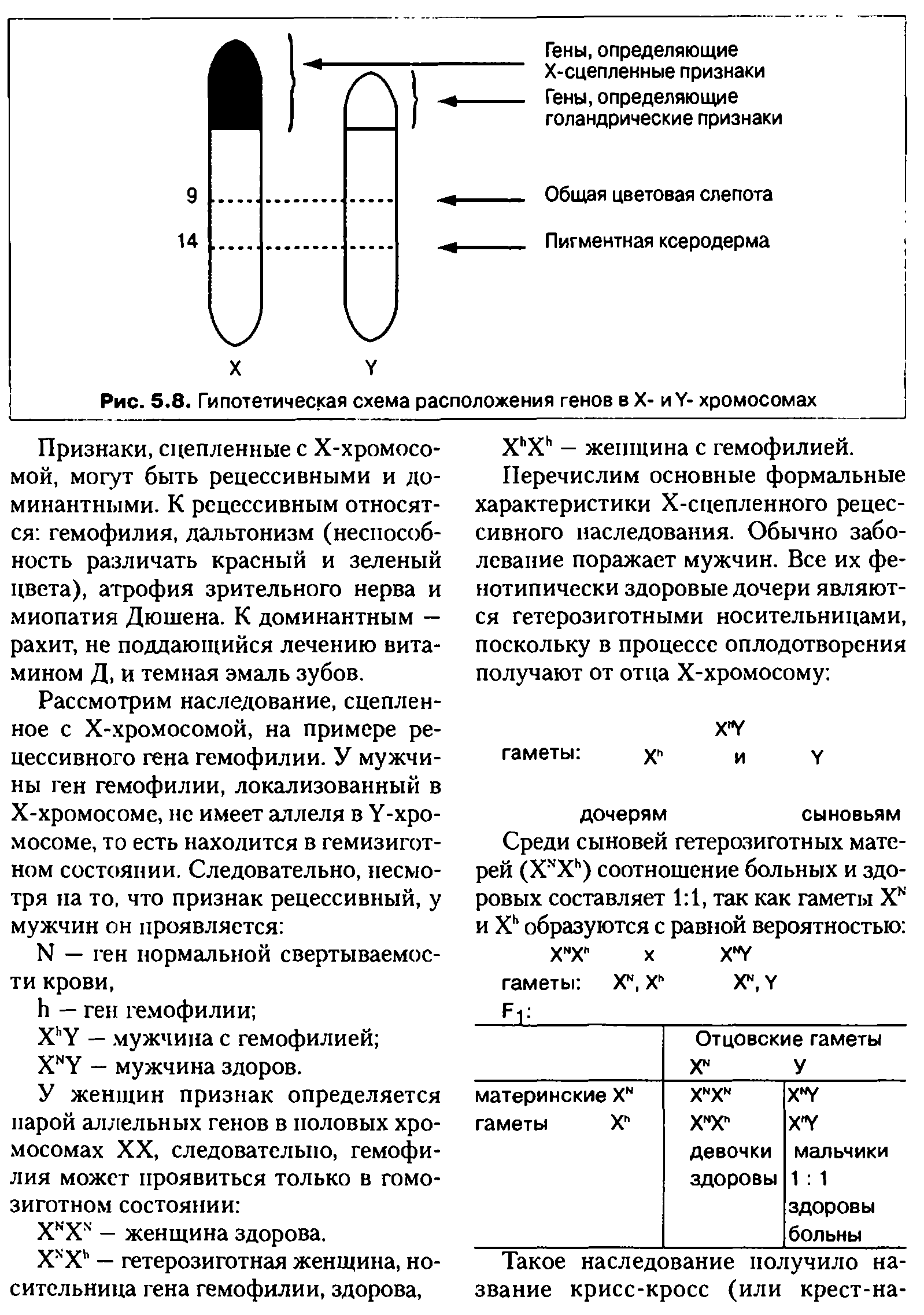
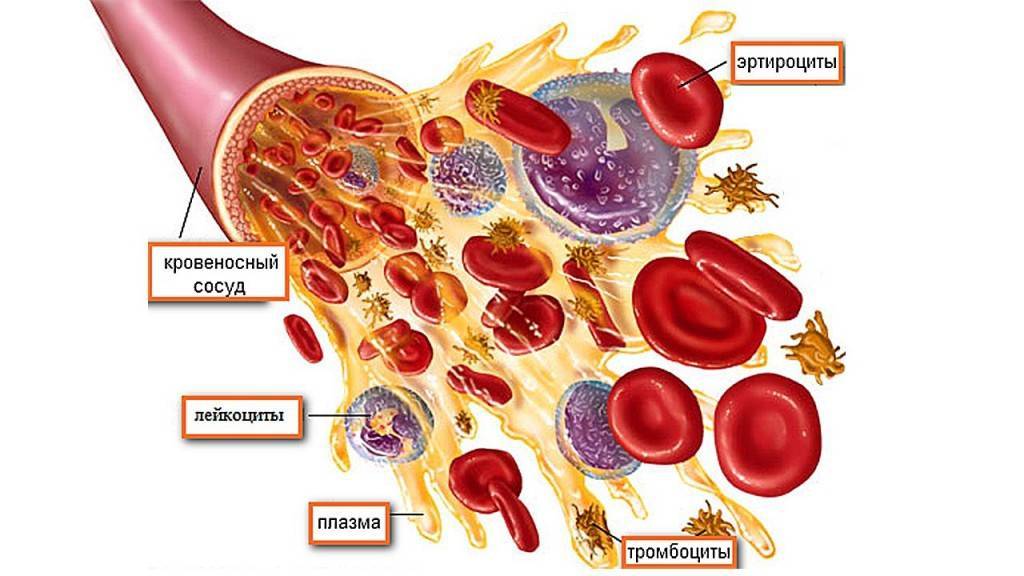
Несмотря на жидкое состояние, кровь является тканевой структурой организма, выполняющей жизненно важные функции. Основные задачи крови — доставка питательных веществ к клеткам, выведение продуктов распада и организация защитных механизмов против чуждых веществ, то есть иммунитет.
Кровь состоит из форменных элементов — клеток и жидкой части — плазмы. Плазма выполняет транспортные функции, доставляя форменные элементы и некоторые питательные вещества. Клетки крови, помимо трофических функций, также обеспечивают иммунные реакции.
Система крови имеет механизм локальной защиты от кровопотери при повреждении сосудов, который обеспечивает образование сгустков, закупоривающих поврежденный просвет. Этот процесс называется свертываемостью или коагуляцией крови, а сам процесс защиты — гемостазом.
Суть гемостаза заключается в концентрации форменных элементов крови в месте повреждения и выделении веществ, способствующих сгущению крови. Основой этого процесса является образование белка фибрина, в нитях которого «запутываются» форменные элементы, образуя плотный сгусток — тромб, который запечатывает отверстие в сосуде.
Гемостаз — сложный биохимический процесс, состоящий из нескольких последовательных стадий. Первая стадия начинается с механического повреждения стенки сосуда, что приводит к проникновению плазмы и форменных элементов в межтканевые пространства, сигнализируя о запуске свертываемости.
Остановка кровотечения происходит в две основные стадии:
-
Первая стадия — первичный сосудисто-тромбоцитарный гемостаз. Она запускает основные механизмы свертывания. В ходе первичного гемостаза происходит рефлекторное сужение поврежденного сосуда и накопление тромбоцитов, что обеспечивает первичную остановку кровотечения, особенно при повреждении мелких сосудов с низким давлением.
-
Вторая стадия — непосредственное свертывание крови, включающее активацию, коагуляцию и ретракцию. Эта стадия важна при значительном повреждении крупных сосудов. Защитная система не может закупорить повреждения в крупных артериях и венах, поэтому без первой медицинской помощи возможна угроза жизни из-за кровопотери.
Свертывание крови на месте первичной тромбоцитарной пробки — это ферментативный и многоступенчатый процесс, завершающийся образованием тромба — твердого образования из нитей фибрина и форменных элементов крови. Ферментативный процесс требует наличия ферментов, основанных на белковых соединениях, для активации каждой стадии.
Если в системе возникают условия, препятствующие образованию хотя бы одного фактора свертывания, гемостаз становится неполноценным или невозможным. Образование сгустка останавливается на той стадии, для которой требуется отсутствующий или функционально слабый фактор.
Факторы свертывания крови, как ферменты, находятся в плазме и тромбоцитах в неактивном состоянии. Повреждения эндотелия сосудов и выход крови в межклеточное пространство стимулируют переход фибриногена в фибрин под воздействием тромбина — взаимодействия фактора свертывания I и II. Далее процесс протекает каскадно и завершается образованием плотного сгустка.
В процессе свертывания участвуют 13 факторов, содержащихся в плазме, и 22 тромбоцитарных фактора.
У здорового человека на первичный гемостаз уходит от одной до трех минут, а на свертывание — до 10-12 минут. Показателем здоровья системы крови является полная остановка кровотечения из мелких сосудов в течение 12 минут. Увеличение этого времени указывает на нарушения в свертывающей системе, а кровотечение, продолжающееся более 30 минут, свидетельствует о серьезных дефицитах факторов свертывания.
Гемофилия — виды болезни
Гемофилия — наследственное заболевание, которое сопровождает человека на протяжении всей жизни. Оно связано с генетической мутацией ряда генов, отвечающих за факторы свертываемости крови и процесс гемостаза.
Генетическое расстройство, вызывающее гемофилию, находится в Х-хромосоме и относится к рецессивным, сцепленным с полом болезням. Чаще всего гемофилия встречается у мужчин, так как у них только одна Х-хромосома. Наличие мутировавшего гена в ней приводит к заболеванию.
Женщины имеют две Х-хромосомы, поэтому вероятность наличия дефектных генов в обеих значительно ниже. Они могут быть носителями гемофилии, но клинические проявления у них обычно отсутствуют. Женщины могут унаследовать дефектные гены от родителей или получить мутацию в своем организме.
Генные дефекты приводят к дефициту определенных факторов свертывания крови или их функциональной недостаточности. При травме кровеносного сосуда не образуется достаточное количество фибрина, необходимого для формирования тромба, что вызывает длительное кровотечение даже из небольших повреждений кожи или внутренних органов. Это может привести к значительной кровопотере и летальному исходу.
Современная гематология использует термины, описывающие временные интервалы, необходимые для формирования различных этапов свертывания крови. Выделяют протромбиновое, тромбиновое и тромбопластиновое время.
Гемофилию делят на несколько видов в зависимости от дефекта в гене. Первые два типа являются рецессивными и зависят от Х-хромосомы, а последний — аутосомно-генетическим, то есть не связан с Х-хромосомой:
- Гемофилия А — наиболее распространенная форма болезни, связанная с отсутствием функционала фактора свертываемости VIII (антигемофильного глобулина). Этот фактор стимулирует протеолиз фактора X с участием фактора IX.
- Гемофилия В — вызвана мутацией гена, отвечающего за функциональность фактора IX (фактора Кристмаса), который зависит от VIII и X факторов свертываемости. Частота гемофилии типа В составляет около 20% от общего числа случаев.
- Гемофилия С — может вызывать повышенную кровоточивость у гетерозиготных пациентов и связана с фактором XI (фактором Розенталя). Носителями и страдающими этим типом заболевания часто являются евреи ашкенази, проживающие в Восточной Европе. У этого типа заболевания частота проявлений одинакова для мужчин и женщин.
Причины развития гемофилии — вероятность наследования от родителей
Гемофилия у пациента обусловлена исключительно наследственностью, и заболевание невозможно приобрести в течение жизни. Симптомы болезни проявляются с первых дней после рождения и остаются неизменными на протяжении всей жизни.
Наиболее распространенные типы гемофилии — А и В — вызваны генной мутацией в Х-хромосоме. Y-хромосома мужчин не содержит генов, отвечающих за свертываемость крови VIII и IX, но в ней присутствуют маскирующие гены, которые могут предотвращать проявление болезни. Отсутствие таких генов в Y-хромосоме приводит к развитию гемофилии у мужчин.
Вероятность заболевания гемофилией у мужчин составляет 50%, если они получают одну Х-хромосому от матери-носительницы (с дефектным геном), и 100%, если мать страдает гемофилией и обе ее Х-хромосомы содержат мутацию.
Вероятность гемофилии у женщин низка, так как обе их Х-хромосомы должны быть дефектными. Это возможно только в случае, если мать страдает гемофилией или является носительницей, а отец болен этим заболеванием.
Однако носительство дефектного гена у женщин может проявляться. Носительницы гемофильных мутаций могут испытывать меноррагию и иметь повышенную склонность к кровоточивости, а также цветовую слепоту.
Матери-носительницы дефектного гена гемофилии передают его дочерям в половине случаев, в то время как отцы, страдающие гемофилией, передают его своим дочерям с вероятностью 100%. Сыновья не могут наследовать гемофилию от отцов, так как болезнь имеет рецессивный тип.
Рекомендуется генетическое тестирование и консультирование для семей, где мужья болеют, а жены являются носительницами дефектного гена. Для раннего выявления гемофилии у плода доступна пренатальная диагностика с использованием амниотической жидкости для генетического исследования. Современные ДНК-анализы могут с почти 100%-ой точностью подтвердить носительство или заболевание гемофилией у плода.
Тяжесть клинического проявления болезни зависит от функциональности факторов свертывания крови — различают легкую и тяжелую формы. Существует также редкая тяжелая форма, при которой факторы свертываемости могут полностью отсутствовать.
Симптомы заболевания и особенности течения гемофилии
Симптомы гемофилии зависят от тяжести заболевания, но общая картина у всех форм болезни схожа — это образование очагов длительного кровотечения в местах травм или самопроизвольно. Такие очаги называют кровоточинами. Пациенты с тяжелой формой гемофилии страдают от более частых и серьезных кровоточин, тогда как у пациентов с легкой формой наблюдаются незначительные симптомы, возникающие после глубоких ранений или хирургических вмешательств. Умеренная форма болезни проявляется симптомами, находящимися между тяжелой и легкой формами.
Гемофилии А и В характеризуются спонтанными кровотечениями с нормальным протромбиновым и тромбиновым временем, но с затяжным тромбопластиновым. Внутренние кровотечения чаще встречаются у пациентов с тяжелой формой болезни и иногда — с умеренной. Наиболее распространенным типом внутренних кровотечений являются суставные, когда кровь скапливается в суставных сумках и перисуставном пространстве.
Этот патологический феномен является одним из самых серьезных и возникает без видимых причин. Накопление крови в суставных полостях значительно ухудшает функциональность сустава и может привести к деструктивным изменениям и ампутации без своевременной медицинской помощи.
Кровотечения в мышцы и мягкие подкожные ткани имеют более благоприятный исход, так как пространство для накопления крови не ограничено, однако также требуют серьезного терапевтического вмешательства.
При рождении ребенка с гемофилией симптомы могут отсутствовать. В некоторых случаях родители узнают о заболевании только после травмы наружных кожных покровов или во время обрезания, если семья исповедует соответствующую религию.
Первыми клиническими проявлениями у детей могут быть многочисленные подкожные гематомы, возникающие даже при незначительных падениях, особенно в период, когда ребенок учится ходить. Легкая форма гемофилии часто протекает незаметно в первые годы жизни и проявляется во время первых посещений стоматолога или при образовании глубоких ран.
Диагностика гемофилии на ранних стадиях
В развитых странах Европы и США представителям семей, планирующих завести ребенка, предлагается базовое обследование на носительство гемофилии. Это помогает снизить рождаемость детей с гемофилией, что улучшает качество жизни родителей и их будущих детей. К сожалению, в нашей стране такая практика отсутствует, хотя пройти необходимые обследования на коммерческой основе не запрещено.
Самым ранним методом диагностики гемофилии является информация о болезни отца и носительство матери. На втором месте стоит ДНК-диагностика околоплодной жидкости во время беременности. Для точного диагноза могут потребоваться образцы крови родственников I и II степени родства.
Независимо от проведенных лабораторных исследований, включая генетическое, гемофилию необходимо дифференцировать от заболеваний и расстройств с похожей клинической картиной нарушения свертываемости крови:
- Гиповитаминоз и авитаминоз К — витамина, участвующего в свертывании крови.
- Болезнь фон Виллебранда, связанная с нарушениями аутосомно-доминантной передачи гемостатических факторов.
- Дисфункция тромбоцитов, например, при тромбастении Гланцманна.
- Дефициты других факторов свертывания крови ненаследственной этиологии — факторов V, VII, X, XI или фибриногена.
- Приобретенная гемофилия.
- Болезнь Элерса-Данлоса.
- Жесткое обращение с детьми и другие расстройства системы крови, влияющие на свертываемость.
Современные способы симптоматического лечения гемофилии
В некоторых случаях у больных гемофилией в крови образуются антитела, которые мешают нормальной работе вливаемых факторов. В таких ситуациях увеличивают дозировку или используют рекомбинантные препараты, полученные из крови животных.
Если организм становится невосприимчивым к факторам свертывания из-за повышения уровня иммунных ингибиторов в плазме, возможно применение рекомбинантного человеческого фактора VII — «New Seven», который является продуктом генной инженерии и широко используется в разных странах по показаниям.
Одним из самых инновационных методов поддержания свертываемости крови при гемофилии является антигемофильный фактор, полученный из клеток яичников китайского хомячка, открытый в начале 2008 года в США. Однако этот препарат используется сравнительно редко из-за высокой стоимости — требуется много хомячков для обеспечения свертываемости крови у одного пациента.
Все методы вливаний факторов свертывания крови применяются не только для лечения в момент кровотечения, но и для профилактики внутренних кровотечений, особенно при умеренной и тяжелой формах болезни. Профилактика включает постоянное наличие факторов свертывания в плазме для предотвращения эпизодов стихийных кровотечений.
Возможные осложнения заболевания и профилактика кровотечений
Основой профилактики кровоточин является обеспечение атравматичности у пациентов. Рекомендуются специальные физические упражнения для укрепления суставов, особенно локтевых, коленных и лодыжек, так как они чаще всего подвержены спонтанным неконтролируемым кровотечениям.
Профилактическое внутривенное введение недостающих или слабо функциональных факторов свертывания — основной способ предотвращения кровотечений при гемофилии.
Осложнения гемофилии часто проявляются при тяжелой форме болезни и реже — при умеренной. К основным осложнениям относятся:
-
Длительное внутреннее кровотечение, образующее полость, заполненную кровью в волоконной структуре скелетных мышц. Это приводит к нарушению их сократительной способности и сдавливанию нервных окончаний.
-
Гемартроз, или гемофилия суставов, — одно из самых частых проявлений гемофилии. Накопление крови в суставной полости вызывает воспаление тканей и дистрофические изменения, сопровождающиеся сильной болью.
Гемартроз обусловлен пролиферативным синовитом, что приводит к разрушению хрящевой ткани. Если не произвести сброс накопившейся крови из суставной полости, это может вызвать апоптоз хондроцитов и разрушение синовиальной ткани. Осадок железа в синовиальной оболочке вызывает воспалительную реакцию и активирует иммунные силы, что усугубляет патологический процесс. Суставные поверхности, лишенные хрящевой оболочки, теряют подвижность, что ведет к разрушению костной основы сустава.
Также возможно заражение крови пациента инфекциями, проникающими в организм при частых вливаниях факторов или переливании крови.
Встречаются побочные реакции со стороны иммунной системы, связанные с производством антител, ингибирующих функциональность сторонних факторов свертывания. Внутричерепное кровоизлияние при гемофилии — одно из самых тяжелых осложнений болезни, способное привести к летальному исходу.
Источник: www.operabelno.ru