| Процедуры и операции | Средняя цена |
| Неврология / Консультации в неврологии | от 500 р. 958 адресов |
| Неврология / Диагностика в неврологии / МРТ в неврологии | от 2000 р. 334 адреса |
| Неврология / Диагностика в неврологии / ЭФИ нервно-мышечной системы | от 400 р. 149 адресов |
| Отоларингология / Диагностика ЛОР-органов / Исследование слухового анализатора | от 100 р. 574 адреса |
| Диагностика / МРТ | от 2350 р. 192 адреса |
| Отоларингология / Диагностика ЛОР-органов / Исследование вестибулярного анализатора | от 80 р. 155 адресов |
| Неврология / Диагностика в неврологии / ЭФИ нервно-мышечной системы | от 500 р. 37 адресов |
| Хирургия / Госпитализация | 10324 р. 126 адресов |
| Диагностика / МРТ / МРТ головы | от 1500 р. 68 адресов |
Источник: www.KrasotaiMedicina.ru
Рассеянный склероз — менее распространенное заболевание по сравнению с сердечно-сосудистыми заболеваниями и онкологией, которые являются основными причинами смерти. О них говорят чаще, и люди знают, на какие симптомы обращать внимание и какой прогноз ожидать. Рассеянный склероз часто становится известен пациентам только от врача, и они не понимают, с чем столкнутся.
В этом материале мы обсудим причины рассеянного склероза и расскажем, у кого он встречается чаще.
Эпидемиология рассеянного склероза
Распространенность рассеянного склероза варьирует в разных регионах. ВОЗ и Международная Федерация Рассеянного Склероза составляют атлас, отражающий частоту заболевания.
В среднем по миру это около 33 случаев на 100 тысяч человек (данные 2013 года). В России распространенность колеблется от 20 до 60 случаев на 100 тысяч, что ставит россиян в зону высокого риска.
Распространенность делится на три зоны:
- Высокого риска (более 50 случаев на 100 тысяч): север США, юг Канады, юго-восточная Австралия, северная Европа. Например, в Северной Америке — 140 случаев на 100 тысяч, в Швеции — 189 случаев.
- Умеренного риска: южная и восточная Европа, юг США, часть южной Америки, остальные регионы Австралии. Например, в Албании — 22 случая на 100 тысяч, что является самым низким показателем в Европе.
- Низкого риска (менее 10 случаев на 100 тысяч): большинство стран Южной Америки, Азии и Африки. В Японии — всего 2–6 случаев на 100 тысяч.
Существует гипотеза о зависимости распространенности от географической широты: чем дальше от экватора, тем выше риск. Однако есть исключения, например, Япония, где рассеянный склероз встречается редко, несмотря на схожую широту с высокорисковыми странами. Миграция также влияет на эту тенденцию: восприимчивость к заболеванию сохраняется при переезде. Например, японцы, живущие в США, болеют реже, чем местные жители. Высокая распространенность в Америке связана с европейскими переселенцами, так как коренные американцы практически не страдают от этого заболевания. Таким образом, наблюдается зависимость от расы: европеоиды более подвержены рассеянному склерозу.
Женщины болеют рассеянным склерозом чаще, чем мужчины — это характерно для большинства аутоиммунных заболеваний. В среднем на одного мужчину с РС приходится две женщины с этим диагнозом. Диспропорция увеличивается, возможно, из-за изменений в репродуктивном поведении и экологических факторов. Однако первично-прогрессирующий РС не подвержен этой тенденции, соотношение составляет 1:1.
Средний возраст начала ремиттирующих форм — 29–32 года. В этом возрасте у многих появляются дети и начинается стабильная карьера, и болезнь вносит коррективы. У женщин средний возраст дебюта РС на 5 лет меньше. Первично-прогрессирующий рассеянный склероз обычно дебютирует в возрасте 35–39 лет. Однако болезнь может начаться как раньше, так и позже: около 5 % случаев — до 18 лет, чаще в пубертатный период; от 3 до 12 % случаев — старше 50 лет.
Что касается продолжительности жизни, рассеянный склероз сокращает ее в среднем на 7–14 лет. В 50 % случаев причиной становятся инфекционные осложнения, которые тяжело переносятся пациентами с неврологическими заболеваниями. За последние десять лет с введением болезни-модифицирующей терапии продолжительность жизни увеличилась на 50 %. Новые методы лечения могут дать еще лучшие результаты.
Этиология рассеянного склероза
Этиология рассеянного склероза до сих пор не полностью изучена, но выявлены факторы, способствующие развитию заболевания.
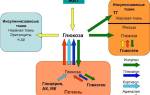
Рисунок 1 | Потенциальные причины этиопатогенеза рассеянного склероза. Источник: Mechelli R. et al. Multiple sclerosis etiology: beyond genes and environment //Expert review of clinical immunology. – 2010
Во-первых, существует наследственная предрасположенность к рассеянному склерозу, имеются семейные случаи. Однако конкордантность монозиготных близнецов составляет всего 30 %, что указывает на значимость других факторов. Современные исследования по эпигенетике показывают, что интерес представляют не только гены, но и механизмы реализации наследственного материала.
- Среди генов, изменения в которых ассоциированы с рассеянным склерозом, в первую очередь выделяются гены главного комплекса гистосовместимости, что характерно для аутоиммунных заболеваний. В дальнейшем этот список пополнили гены, найденные в ходе полногеномного поиска ассоциаций (GWAS):
- Многие из них связаны с работой иммунной системы: гены, участвующие в антигенной презентации, сборке лектинов, рецепторов к цитокинам и простагландинам, интерферонам 1 типа, а также дифференцировке и ко-стимуляции Т-лимфоцитов.
- Гены, необходимые для функционирования нейронов, например, при аксональном транспорте и дифференцировке нейронов.
- Гены, регулирующие общие функции клеток, такие как апоптоз и клеточная адгезия.
- Один из генов, необходимых для метаболизма витамина D.
Вклад каждой отдельной мутации в этих генах оказывается мал, и поиски концепции, объясняющей генетическую основу рассеянного склероза, продолжаются. Обнаружено, что имеет значение, от какого родителя унаследован ген, то есть существует эффект импринтинга.
- Роль в генетической предрасположенности может играть альтернативный сплайсинг. Исследования проводились на мышах с экспериментальным аутоиммунным энцефаломиелитом, моделью рассеянного склероза. Выявлены гены, которые подвергаются сплайсингу иначе у устойчивых к заболеванию линий; эти гены участвуют в межклеточной коммуникации и регуляции транскрипции.
Продукт транскрипции гена IL-7R-альфа вызывает альтернативный сплайсинг, что приводит к повышению продукции растворимой формы IL-7R-альфа и предрасположенности к активному функционированию путей иммунного ответа.
- МикроРНК могут быть еще одним звеном в развитии предрасположенности и целью для лечения. Они участвуют в посттранскрипционном процессинге, подавляя трансляцию. Известно, что эта функция нарушена при злокачественных опухолях, и разрабатывается терапия на основе РНК-интерференции. МикроРНК также регулируют развитие иммунных клеток и воспалительный ответ.
Уже проведены исследования, выявившие три микроРНК, связанные с развитием ремиттирующего РС; одна из них, miRNA-145, с 89 % специфичностью отличает больного с РС от здорового. Обнаружены 165 типов микроРНК, функционирующих при РС иначе, чем у здоровых.
- Эпигенетические процессы могут влиять на экспрессию генов главного комплекса гистосовместимости.
Показано, что ингибитор гистондеацетилазы трихостатин А индуцирует транскрипцию гена MHC II DRA и изменяет функционирование класса II генов главного комплекса гистосовместимости. Предполагается, что их работа контролируется ацетилированием гистонов.
Также высказывалась гипотеза о том, что при РС может изменяться активность промотора гена MCH2TA, активатора транскрипции генов комплекса MHC второго класса. Однако при исследовании клеток крови дискордантных по РС монозиготных близнецов отличий не обнаружено; предполагается, что нужно исследовать и другие ткани.
Эпигенетические процессы могут лежать в основе повреждения олигодендроцитов при РС. Здесь речь идет о патогенезе уже развившегося заболевания, но они также относятся к реализации генетической информации.
Нормальное белое вещество (NAWM) может быть поврежденным; нарушения в его формировании и структурные отличия связаны с дефектностью миелина. Уровень цитруллинирования миелина коррелирует с тяжестью заболевания и происходит из-за гипометилирования промотора пептидиларгининдезаминазы 2 типа (PAD2), который превращает аргинин в цитруллин.
Цитруллин может образовываться из аргинина и на остатках гистонов — еще одного звена эпигенетического контроля. Высокий уровень цитруллинирования гистонов H3 обнаружен у пациентов с РС и у мышей с экспериментальным энцефалитом. Этот процесс опосредуется PAD 4 типа, которая при рассеянном склерозе мигрирует в ядро под действием ФНО-альфа. Изменения в структуре хроматина, вызванные цитруллинированием, могут приводить к апоптозу олигодендроцитов.
Во-вторых, реализация наследственной предрасположенности к аутоиммунным заболеваниям может зависеть от вирусных заболеваний. Исследована связь рассеянного склероза с инфекциями, такими как вирус Эпштейна-Барр, герпесвирус 6 типа, Chlamydia pneumoniae и микобактерии.
Вирусом Эпштейна-Барр инфицирована большая часть населения, и среди больных РС этот показатель составляет 99 %. Есть данные о том, что РС чаще встречается у перенесших инфекционный мононуклеоз. Механизм может заключаться в персистировании вируса, что приводит к образованию менингеальных узелков с B-клетками, которые также обнаруживаются в активных бляшках. Вирус влияет на реализацию генетической информации в В-клетках, где он может длительное время оставаться интегрированным с клеточным геном.
Также в активных бляшках обнаруживают герпесвирус 6 типа, который может иметь перекрестные антигены с белками миелина.
Кроме того, существуют эндогенные человеческие ретровирусы. Их гены редко играют важную роль, но, например, ген синцитина-1, медиатора проникновения трофобласта, повышается в нервной ткани у пациентов с РС. В спинномозговой жидкости обнаруживают РНК эндогенного ретровируса (MSRV), а в сыворотке — сам синцитин. Географическая карта распространенности MSRV совпадает с картой распространенности РС. Активация эндогенных ретровирусов может быть связана с инфицированием нейротропными герпесвирусами.
В-третьих, обсуждается роль витамина D в генезе различных патологий, включая рассеянный склероз. Обнаружено, что витамин D взаимодействует с локусом HLA-DR2, связанным с предрасположенностью к РС, изменяя экспрессию антигена на поверхности антиген-презентирующих клеток.
В-четвертых, образ жизни и средовые факторы, такие как курение, диета и инсоляция, могут влиять на развитие и тяжесть РС.
Источники:
- Bradley’s Neurology in Clinical Practice, 7th Edition (2016)
- Lutton J. D., Winston R., Rodman T. C. Multiple sclerosis: etiological mechanisms and future directions //Experimental biology and medicine. — 2004. — Т. 229. — №. 1. — С. 12–20.
- Mechelli R. et al. Multiple sclerosis etiology: beyond genes and environment // Expert review of clinical immunology. — 2010. — Т. 6. — №. 3. — С. 481–490.
- The MSIF Atlas of MS 2013 [Электронный ресурс]. – Режим доступа : http://clc.to/gbYE1Q, свободный. – Загл. с экрана.
Источник: medach.pro
Лечение рассеянного склероза.
Основная задача лечения — уменьшение активности патологического процесса в период обострения и острого течения заболевания.
Для этого применяют высокие дозы кортикостероидов (преднизолон, дексаметазон) и АКТГ. Преднизолон назначают внутрь в интенсивных или подавляющих дозах в зависимости от активности заболевания. Интенсивная доза составляет 0,75 мг/кг в сутки, которую принимают в 1 или 2 приема утром. Глюкокортикоиды могут назначаться ежедневно или через день; курс лечения длится 2—3 недели, после чего дозу постепенно уменьшают в течение 2—3 месяцев.
Одновременно назначают анаболические гормоны (неробол, ретаболил), препараты калия и кальция, аскорбиновую кислоту, верошпирон. Ретаболил вводят внутримышечно по 50 мг 1—2 раза в неделю, на курс 25—30 инъекций. Нерабол принимают по 1—2 таблетки 2 раза в день, суточная доза — 10—20 мг; верошпирон — по 25 мг 2 раза в день, суточная доза — 50 мг.
Подавляющие дозы преднизолона назначают по непрерывной (ежедневно) или прерывистой (через день) схеме, в зависимости от тяжести процесса. Максимальная суточная доза при непрерывной схеме — до 1,5 мг/кг. После достижения терапевтического эффекта дозу постепенно снижают. При прерывистой схеме суточную дозу делят на две равные части: первую принимают утром после завтрака, вторую — через час. В последние годы с хорошим эффектом применяют высокие дозы метилпреднизолона (10—15 мг/кг в сутки) внутривенно 3—4 раза в сутки в течение 3—5 дней, затем переходят на таблетированную форму через день (1 мг/кг). Дозу постепенно уменьшают до полной отмены.
Лечение АКТГ проводят в дозе 1000 ЕД на курс, суточная доза для внутримышечного введения — 40—60 ЕД. При обострении возможно применение этимизола по 100 мг 3 раза в день в течение 1,5—2 месяцев. Больным с прогрессирующим течением болезни назначают левамизол по 150 мг в день в течение 3 дней каждую неделю на протяжении 3—4 месяцев.
В последние годы для лечения рассеянного склероза начали использовать иммуномодуляторы: Т-активин (по 100 мкг подкожно ежедневно в течение 5 дней, затем 1—3 инъекции каждые 10 дней) и тималин (по 10 мг внутримышечно 2 раза в сутки в течение 5 дней, затем 1 инъекция каждые 10 дней в течение 1—3 дней). На всех этапах болезни применяются витамины группы В, десенсибилизирующие средства, АТФ, трасилол, церебролизин. Среди симптоматических средств важное место занимают препараты, снижающие мышечный тонус: баклофен, седуксен. При наличии гиперкинезов показаны динезин и нарокин.
Физические методы лечения включают дозированную гимнастику и избирательный массаж. Противопоказаны бальнео- и грязелечение, а также солнечные инсоляции. Больным может быть рекомендовано санаторно-курортное лечение общеукрепляющего типа, не связанное с резким изменением климатических условий.
Лечение должно быть интенсивным не только в период обострения, но и в ремиссии. В последнем случае его проводят 2 раза в год (весной и осенью) с курсами витаминотерапии и биостимуляторов. Это лечение, совместно с мерами по предупреждению инфекций, интоксикаций и переутомления, помогает предотвратить обострения.
Прогноз.
Прогноз в отношении жизни благоприятный, за исключением случаев с острыми бульбарными нарушениями, которые могут привести к летальному исходу. Наблюдаются случаи длительного благоприятного течения, когда больные сохраняют трудоспособность. Однако многие пациенты становятся инвалидами в течение первых 3—5 лет после начала болезни. Поэтому важно правильно и своевременно устанавливать группу инвалидности, что может способствовать более длительной трудоспособности больных.
Патогенез рассеянного склероза (РС) остается не до конца изученным. Он гораздо сложнее, чем считалось ранее. Традиционное представление о РС как хроническом воспалительном заболевании ЦНС с образованием очагов демиелинизации и сохранением аксонов является упрощением.
С внедрением магнитно-резонансной томографии (МРТ) и других методов, а также накоплением патоморфологических данных выяснилось, что:
- Фокальное поражение белого вещества — лишь часть патологии РС; выраженные нарушения наблюдаются и в нормально выглядящем белом и сером веществе, что сопровождается снижением объема мозга.
- Патологические изменения затрагивают не только миелин, но и аксоны, нейроны.
- Прогрессирующее поражение головного мозга может происходить при слабом воспалении [Kutzelnigg A., Lassmann H., 2014].
Механизм повреждения нервной ткани при РС включает два основных процесса: иммуновоспалительную демиелинизацию и нейродегенерацию. Условно выделяют 5 стадий патогенеза [Хайбуллин Т.И., Хабиров Ф.А., Девликамовна Ф.И. и соавт., 2010].
I этап — активация аутореактивных Т-хелперов I типа (Th I). Установлено, что аутореактивные Th не полностью удаляются в тимусе и циркулируют в крови. Предполагается, что генетические факторы придают этим клеткам повышенную способность к активации. Основное значение в развитии аутоиммунного процесса имеют молекулярная мимикрия и расширение эпитопов, что способствует сенсибилизации Th к собственным антигенам. При РС преобладает иммунный ответ, индуцируемый Th I, также установлена роль Th 17 в апоптозе олигодендроцитов и нарушении способности Treg-лимфоцитов подавлять аутоиммунный процесс.
II этап — миграция аутореактивных Th в ЦНС через гематоэнцефалический барьер (ГЭБ). Активированные Th экспрессируют антигены, которые взаимодействуют с молекулами адгезии на эндотелии сосудов, что способствует их проникновению через ГЭБ. Th могут проникать и транцеллюлярно, что указывает на активное взаимодействие нейронов и макроглии с иммунной системой.
III этап — развитие аутоиммунного воспаления. Проникнув в ЦНС, Th активируются, пролиферируют и секретируют провоспалительные цитокины, что запускает каскад воспалительных процессов. Это приводит к повышению проницаемости ГЭБ и миграции макрофагов, цитотоксических лимфоцитов и B-лимфоцитов, а также активации микроглии.
IV этап — воспалительный демиелинизирующий процесс. Активированные B-лимфоциты секретируют олигоклональные иммуноглобулины класса G (Ig G), которые повреждают миелиновую оболочку и олигодендроциты. Цитотоксические Т-лимфоциты CD8+ также вызывают гибель аксонов. Выделяют 4 механизма демиелинизации: макрофаг-ассоциированная, антителоиндуцированная, дистальная олигодендропатия и первичная олигодендроцитарная дегенерация.
V этап — процесс ремиелинизации. С течением времени активность воспалительного процесса снижается, и начинается ремиелинизация, обеспечиваемая активацией клеток-предшественников олигодендроцитов. Однако ремиелинизация при РС несовершенна, что приводит к меньшей толщине миелина и сниженной скорости проведения нервного импульса.
Основным патоморфологическим проявлением РС являются очаги воспалительной демиелинизации, которые локализуются в различных отделах белого вещества головного и спинного мозга. Размеры бляшек варьируют от нескольких миллиметров до нескольких сантиметров, их количество увеличивается с прогрессированием заболевания. Морфологическое строение бляшек зависит от времени их образования, выделяют свежие и старые бляшки. По мере старения бляшек наблюдаются изменения в нейроглии, приводящие к образованию глиозного рубца.
Наряду с морфологическими изменениями в области бляшек, гистологические изменения обнаруживаются и в неизмененной ткани. Прогрессирует атрофия головного и спинного мозга.
Эпидемиология
Рассеянный склероз — распространенное заболевание, которым страдают не менее 2 миллионов человек по всему миру. Заболевание чаще всего поражает молодых людей до 30 лет. У людей старшего возраста оно встречается реже, а после 50 лет риск заболевания значительно снижается. У детей рассеянный склероз встречается крайне редко.
Женщины болеют этим заболеванием в 1,5 раза чаще мужчин, однако у мужчин чаще диагностируется злокачественная прогрессирующая форма без ремиссий.
Географическое положение также влияет на распространенность заболевания — риск его развития увеличивается с удалением от экватора. Наиболее подвержены заболеванию территории севернее 30 параллели (данные по южным регионам ограничены).
Рассеянный склероз в основном поражает представителей европеоидной расы. Среди монголоидной расы он диагностируется крайне редко: в Японии, Китае и Корее фиксируется не более 6 случаев на 100 тыс. человек; данных по другим расам недостаточно.
Причины рассеянного склероза и патогенез
На сегодняшний день нет точного ответа на вопрос о причинах рассеянного склероза. Однако исследователи выделили несколько факторов, играющих важную роль в его патогенезе.
- Аутоиммунный фактор. В процессе развития заболевания происходит сбой в работе иммунной системы, которая начинает атаковать ткани мозга, разрушая миелиновую оболочку. Неясно, является ли эта реакция первичной или вторичной: иммунный ответ может возникать в ответ на воспаление, или же воспаление и демиелинизация могут быть следствием иммунного ответа.
- Сбой гемато-энцефалического барьера. Эта система защищает мозг от проникновения токсинов, бактерий и иммунных клеток. При рассеянном склерозе барьер нарушается, и иммунные клетки проникают в мозг, атакуя его как чуждый объект. Исследования показывают связь между аутоиммунными процессами в мозге и фибриногеном, белком, отвечающим за свертываемость крови, но характер этой связи пока не установлен.
На развитие заболевания могут влиять различные факторы, связанные с запуском аутоиммунных процессов:
- Вирусы и бактерии. Инфекции, такие как стафилококки, стрептококки, ретровирусы, вирусы кори и герпеса, могут спровоцировать аутоиммунные реакции, хотя сами по себе не являются причиной рассеянного склероза. Латентные инфекции, такие как герпес, особенно опасны, так как могут активироваться при ослаблении иммунной системы.
- Хронические интоксикации. Токсичные вещества могут вызывать иммунный ответ, что становится провоцирующим фактором для заболевания.
- Стрессы. Сильный физический или психический стресс может запустить механизм развития болезни.
- Курение. Курение увеличивает риск развития рассеянного склероза, но механизм этого влияния неясен.
- Уровень мочевой кислоты. У больных рассеянным склерозом отмечается низкий уровень мочевой кислоты, что может указывать на ее защитную роль, но механизм этого эффекта не выяснен.
- Повышенный уровень сахара в крови. Нарушения обмена глюкозы, такие как сахарный диабет, могут стать триггерами аутоиммунной реакции. У диабетиков рассеянный склероз протекает быстрее из-за сниженной регенерации клеток.
- Травмы и хирургические вмешательства. Механические повреждения спинного и головного мозга могут приводить к увеличению выработки лимфоцитов и лейкоцитов, что может вызвать атаку на собственные ткани.
- Авитаминоз. В частности, недостаток витамина D.
- Пищевая аллергия. Аллергия представляет собой патологический иммунный ответ на аллерген, и частое употребление аллергенного продукта может вызвать затяжную иммунную реакцию.
- Чрезмерное употребление животных белков. Связь между потреблением животного белка и риском развития рассеянного склероза установлена, но убедительных доказательств провокации заболевания пока нет.
- Необходимость в качественной питьевой воде. Употребление жесткой и минерализованной воды может быть связано с риском развития болезни, вероятно, из-за хронической интоксикации, активирующей иммунную систему.
Для получения информации о распространенных симптомах заболевания и действиях в период обострения, переходите по ссылке.
Диагностика
Основной метод диагностики – магнитно-резонансная томография (МРТ) головного мозга и позвоночника, поскольку заболевание затрагивает как головной, так и спинной мозг. МРТ позволяет определить локализацию очагов склероза и степень демиелинизации тканей. Наиболее точные результаты достигаются при использовании контрастного вещества.
Дополнительно для подтверждения диагноза проводится анализ спинномозговой жидкости. Повышенное содержание лимфоцитов и миелина указывает на наличие склероза.
Источник: inBrain.top