Врожденные пороки сердца (ВПС) у детей формируются внутриутробно. При этой патологии наблюдается аномальное развитие сердца, клапанов и сосудов. К сожалению, уровень смертности среди детей с ВПС высок, особенно в первый год жизни. Если дети переживают этот критический период, в дальнейшем возможно улучшение состояния, что снижает смертность. По статистике, после достижения ребенком одного года вероятность летального исхода на фоне ВПС составляет менее 7%.
Причины заболевания
Причины врожденных пороков сердца (ВПС) у детей:
- генетическая предрасположенность;
- инфекционные заболевания (например, краснуха);
- употребление наркотиков или алкоголя матерью во время беременности;
- радиоактивное облучение;
- прием антибиотиков матерью в первом триместре беременности.
Существуют и другие факторы, которые могут способствовать развитию порока сердца. К ним относятся возраст беременной женщины (старше 35 лет), эндокринные заболевания у одного из родителей, тяжелая беременность и нарушения гормонального фона.
Признаки и симптомы ВПС у детей
Аномальное развитие сердца можно выявить уже на сроке 4-5 месяцев беременности при УЗИ. Диагноз подтверждается или опровергается вскоре после рождения. Иногда, особенно при дефекте межпредсердной перегородки (ДМПП), заболевание трудно диагностировать из-за отсутствия видимых симптомов. В таких случаях человек может узнать о диагнозе случайно, например, при медицинской комиссии на работе во взрослом возрасте.
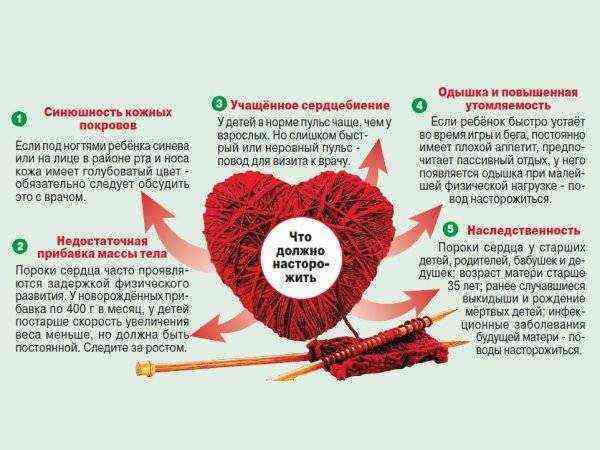
Симптомы врожденных пороков сердца (ВПС) включают:
- бледный цвет кожи с синюшным оттенком на носу, губах и ушах;
- холодные конечности;
- плохую динамику набора веса;
- шумы в сердце;
- вялость и затрудненное дыхание.
Дети с ВПС хуже переносят физические нагрузки, быстро утомляются и могут часто терять сознание. При появлении негативных симптомов необходимо обратиться к врачу для комплексного обследования, включая электрокардиограмму и эхографию сердца. Болезни сердца опасны, но своевременная диагностика и правильное лечение могут значительно повысить шансы на полноценную жизнь.
Классификация врожденных пороков сердца включает:
- тетрада Фалло;
- дефект межпредсердной перегородки;
- открытый артериальный проток;
- коарктация аорты;
- ДМПП;
- стеноз устья аорты и другие.
Существует более 100 врожденных сердечных пороков, но некоторые из них схожи по природе и способу лечения, поэтому объединены в подгруппы.
Дефект межпредсердной перегородки (ДМПП)
ДМПП — это врожденный порок сердца, связанный с аномальным развитием межпредсердной перегородки. При этом образуется отверстие, через которое смешиваются кровь из левого и правого предсердий.
Существует два типа дефектов: первичный и вторичный. Первичный дефект находится в нижней части перегородки, а вторичный — в области овального окна или впадения нижней полой вены. Чаще всего встречается вторичный дефект.
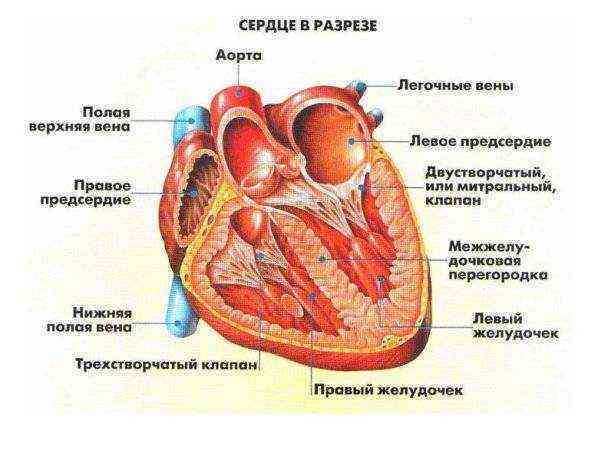
Сердце человека состоит из четырех камер: правого и левого предсердий, правого и левого желудочков. Кровь, обогащенная кислородом в легких, попадает в левый желудочек и выбрасывается в аорту. Оттуда она разносится по организму, питая органы и ткани, забирая углекислый газ и возвращаясь в правое предсердие в виде венозной крови. Затем венозная кровь поступает в правый желудочек и через легочную артерию направляется в легкие для обмена углекислого газа на кислород.
При ДМПП нормальная циркуляция крови нарушается, так как происходит смешивание крови между предсердиями. В норме давление в левом предсердии выше, чем в правом, что приводит к сбросу крови слева направо.
У детей первого года жизни диагностировать ДМПП сложно, так как давление в предсердиях практически одинаково. С возрастом, с увеличением физической нагрузки, давление в левом предсердии возрастает, что увеличивает заброс крови через отверстие и может привести к легочной гипертензии, чаще всего развивающейся в зрелом возрасте. Симптомы могут отсутствовать, и заболевание часто обнаруживается случайно при обследовании.
Родители могут заметить у ребенка повышенную утомляемость, тахикардию, одышку, увеличение печени и сердечный горб. При обычном прослушивании сердца шум может не обнаруживаться, как и при кардиограмме, где показатели могут быть в норме. При выраженном ДМПП могут наблюдаться перегрузки правых отделов и нарушения ритма.
Диагностика ДМПП осуществляется с помощью эхокардиографии, которая позволяет определить локализацию и размер дефекта, а также область заброса крови.
Дети в возрасте от 1 до 4 лет могут справиться с недугом без операции, так как межпредсердная перегородка может самопроизвольно закрыться или уменьшиться до такого размера, что не нарушает кровообращение. Взрослым лечение ДМПП без хирургического вмешательства невозможно. Раннее проведение операции снижает риск легочной гипертензии, тромбообразования и инсульта.
Медикаментозное лечение направлено на снижение нагрузки на правые отделы сердца. Оперативное лечение может быть выполнено двумя способами:
-
Операция на открытом сердце с полным вскрытием грудной клетки. Обеспечивается искусственное кровообращение, что позволяет органам функционировать нормально. В ходе операции дефект перегородки ушивается или закрывается специальной заплаткой.
-
Эндоваскулярная операция. Закрытие дефекта производится с помощью окклюдера, что позволяет избежать вскрытия грудной клетки и обеспечивает более быстрое восстановление.
Дети быстрее восстанавливаются после хирургического лечения, и заплаточная перегородка вскоре зарастает тканью, что позволяет вести активную жизнь без страха преждевременной смерти.
Открытый артериальный проток
Открытый артериальный проток (ОАП) чаще всего встречается у недоношенных детей. В норме он обеспечивает кровообращение плода в утробе матери, но после рождения должен закрываться в течение первых дней у доношенных детей и в течение недели у недоношенных. При ОАП этот процесс не происходит, и заболевание можно диагностировать примерно в 2-3 месяца.
Симптомы ОАП включают тяжелое дыхание, плохую прибавку в весе, бледность кожи, затруднения при кормлении и повышенную потливость. В более старшем возрасте дети с ОАП могут быть худыми, иметь сиплый голос, часто болеть простудами и отставать в умственном и физическом развитии от сверстников.
Лечение ОАП у детей до трех месяцев обычно не требуется, так как артериальный проток может закрыться самостоятельно. Если этого не происходит, применяются медикаменты, катетеризация или перевязка протока.
На ранних стадиях возможно лечение с помощью местных препаратов: мочегонных, антибактериальных и нестероидных противовоспалительных средств.
Катетеризация протока является одной из самых эффективных и безопасных процедур, так как выполняется через крупную артерию, а не через грудную клетку. Она показана детям старше одного года, если консервативное лечение не дало результатов.
Хирургическое лечение ОАП включает перевязку артерии. Его рекомендуется проводить до трехлетнего возраста, чтобы минимизировать риск послеоперационных осложнений.
Гипоплазия левых отделов сердца
ГЛОС, или гипоплазия левых отделов сердца, относится к врожденным порокам сердца (ВПС). При этой патологии наблюдается недоразвитие левого желудочка и его слабая функциональность. ГЛОС встречается редко, но является одной из причин гибели маленьких детей. Другие названия болезни — синдром Раухфуса-Киселя. Основными причинами возникновения являются наследственные факторы и раннее закрытие овального окна. При гипоплазии могут также наблюдаться недоразвитие межпредсердной и межжелудочковой перегородок.
Диагностировать патологию можно на пятом месяце беременности. На этом сроке будущей маме назначают медикаменты для улучшения состояния ребенка. Раннее выявление патологии с помощью УЗИ позволяет направить новорожденного в специализированную клинику для лечения ВПС. Оперативные меры и своевременное лечение могут сохранить здоровье и жизнь ребенка.
Основная задача лечения ГЛОС у новорожденных — предотвратить закрытие артериального протока и попытаться его открыть. Ранее дети с ГЛОС считались обреченными, так как не существовало эффективных методов лечения. Хотя риск летального исхода остается высоким, сейчас есть возможность спасения.
Для лечения ГЛОС применяют три вида хирургического вмешательства: операция Норвуда, операция Гленна и операция Фонтена. Однако исход после операции не всегда благоприятный: выживает около 65% детей, и 90% из них погибают до достижения первого месяца жизни.
Лечение ВПС у детей чаще всего включает хирургическое вмешательство, а консервативная терапия используется как вспомогательное средство для поддержания состояния до и после операции. Если ВПС незначителен и не вызывает серьезных проблем, проводится наблюдение за состоянием сердца и внутренних органов, а при необходимости назначается соответствующая терапия.
Для профилактики ВПС важно внимательно относиться к своему здоровью в период планирования беременности и во время самой беременности. Если в семье есть случаи сердечно-сосудистых заболеваний, необходимо сообщить об этом гинекологу. Также следует осторожно подбирать медикаменты в первом триместре беременности и избегать самостоятельного назначения препаратов.
Врожденный порок сердца №1: двустворчатый клапан аорты
При неосложненном течении этого врожденного порока сердца лечение не требуется, физическая активность не ограничивается. Обязательными мерами профилактики являются ежегодный осмотр у кардиолога, а также профилактика инфекционного эндокардита и атеросклероза.
Врожденный порок сердца №2: дефект межжелудочковой перегородки
Дефект межжелудочковой перегородки — это врожденный порок, при котором перегородка между правым и левым желудочками сердца имеет «окно». Это приводит к смешению артериальной и венозной крови, что не должно происходить в здоровом организме.
Дефект межжелудочковой перегородки занимает второе место по частоте среди врожденных пороков сердца, встречаясь у 0,6% новорожденных. Он часто сочетается с другими аномалиями сердца и сосудов и одинаково распространен среди мальчиков и девочек. Возникновение дефекта может быть связано с сахарным диабетом или алкоголизмом у матери. К счастью, «окно» часто закрывается спонтанно в течение первого года жизни, и при нормальных показателях работы сердечно-сосудистой системы ребенку не требуется наблюдение у кардиолога или ограничение физической активности.
Диагноз ставится на основе клинических проявлений и подтверждается эхокардиографией.
Лечение зависит от размера дефекта и наличия клинических проявлений. При небольшом дефекте без симптомов прогноз благоприятный: ребенку не требуется медикаментозное лечение или операция. Однако перед стоматологическими вмешательствами необходима профилактическая терапия антибиотиками для предотвращения инфекционного эндокардита.
При среднем и большом дефекте с признаками сердечной недостаточности показана консервативная терапия с использованием мочегонных, антигипертензивных препаратов и сердечных гликозидов. Хирургическая коррекция требуется при больших дефектах, отсутствии эффекта от консервативного лечения и наличии легочной гипертензии. Обычно операцию проводят до 1 года.
Дети с небольшим дефектом, не требующим операции, находятся под диспансерным контролем у кардиолога и получают профилактическую терапию инфекционного эндокардита. Дети, перенесшие операцию, также должны регулярно (2 раза в год) обследоваться у кардиолога. Степень ограничения физической нагрузки определяется индивидуально на основе обследования.
Сосудистый врожденный порок сердца: открытый артериальный проток
Открытый артериальный (боталлов) проток — распространенный врожденный порок сердца. Это сосуд, через который во внутриутробном периоде сбрасывается кровь из легочной артерии в аорту, минуя легкие, которые не функционируют. После рождения, когда легкие начинают работать, проток закрывается. Обычно это происходит в течение 10 дней жизни доношенного новорожденного, чаще всего через 10-18 часов после рождения. У недоношенных детей открытый артериальный проток может оставаться открытым несколько недель.
Если проток не закрывается в установленный срок, врачи говорят о незаращении аортального протока. Частота этого порока у доношенных детей составляет 0,02%, а у недоношенных и маловесных — 30%. Открытый аортальный проток чаще встречается у девочек. Он может возникать у детей, чьи матери во время беременности перенесли краснуху или злоупотребляли алкоголем. Диагноз ставится на основе специфического сердечного шума и подтверждается эхокардиографией с допплерографией.
Лечение незаращения аортального протока начинается с момента его выявления. Новорожденным назначают нестероидные противовоспалительные препараты (например, индометацин), которые способствуют закрытию протока. Если спонтанное закрытие не происходит, проводится хирургическая коррекция: проток перевязывают или иссекают.
Прогноз для детей с устраненным пороком сердца благоприятный. Они не нуждаются в физических ограничениях или специальном уходе. Однако у недоношенных детей с открытым артериальным протоком могут развиваться хронические бронхолегочные заболевания.
Коарктация аорты
Коарктация аорты — это врожденный порок сердца, характеризующийся сужением просвета аорты, чаще всего вблизи места выхода из сердца. Этот порок занимает 4-е место по распространенности. У мальчиков он встречается в 2-2,5 раза чаще, чем у девочек. Средний возраст диагностики — 3-5 лет. Коарктация часто сочетается с другими аномалиями, такими как двустворчатый аортальный клапан, дефект межжелудочковой перегородки и аневризмы сосудов.
Диагноз устанавливается случайно при обследовании по другим причинам (инфекции, травмы) или во время профосмотра. Подозрение на коарктацию возникает при артериальной гипертензии и специфических шумов в области сердца. Диагноз подтверждается эхокардиографией.
Лечение коарктации аорты — хирургическое. Перед операцией проводится полное обследование и назначается терапия для нормализации артериального давления. Операция выполняется в кратчайшие сроки при наличии симптомов, а при бессимптомном течении — в плановом порядке в возрасте 3-5 лет. Выбор хирургической методики зависит от возраста пациента, степени сужения аорты и наличия сопутствующих аномалий. Риск рекоарктации высок, если сужение составляет 50% и более от нормального просвета аорты.
После операции пациенты нуждаются в регулярном наблюдении детского кардиолога. Многие продолжают принимать антигипертензивные препараты в течение нескольких месяцев или лет. После подросткового возраста пациенты переходят под наблюдение взрослого кардиолога.
Степень допустимой физической активности определяется индивидуально и зависит от компенсации порока, уровня АД и результатов операции. К осложнениям относятся рекоарктация и аневризма аорты.
Прогноз: чем раньше выявлена и устранена коарктация, тем выше продолжительность жизни пациента. Без операции средняя продолжительность жизни составляет около 35 лет.
Безопасный врожденный порок сердца: пролапс митрального клапана
Пролапс митрального клапана — одна из наиболее распространенных сердечных патологий, встречающаяся у 2-16% детей и подростков. Это врожденный порок сердца, при котором створки митрального клапана прогибаются в полость левого предсердия во время сокращения левого желудочка, что приводит к неполному смыканию клапана. В результате может происходить обратный ток крови из левого желудочка в левое предсердие (регургитация), что в норме недопустимо. В последние десять лет, благодаря активному внедрению эхокардиографии, частота выявления пролапса значительно возросла, особенно среди «немых» случаев, которые невозможно было обнаружить при аускультации. Эти пороки часто не имеют клинических проявлений и выявляются во время диспансеризации здоровых детей.
Пролапсы митрального клапана делятся на первичные (не связанные с заболеваниями сердца и патологией соединительной ткани) и вторичные (возникающие на фоне заболеваний соединительной ткани, сердца, гормональных и метаболических нарушений). Чаще всего пролапс диагностируется у детей в возрасте 7-15 лет. До 10 лет он встречается одинаково у мальчиков и девочек, но после 10 лет у девочек он выявляется в 2 раза чаще.
Частота пролапса повышается у детей, чьи матери имели осложненное течение беременности (особенно в первые 3 месяца) или патологические роды (быстрые, стремительные роды, кесарево сечение по экстренным показаниям).
Клинические проявления варьируют от минимальных до выраженных. Основные жалобы включают боли в области сердца, одышку, сердцебиение, слабость и головные боли. У пациентов с пролапсом часто наблюдаются психоэмоциональные нарушения, особенно в подростковом возрасте, в виде депрессивных и невротических состояний.
Диагноз ставится на основании клинической картины и аускультации, а подтверждается эхокардиографией. Выделяют 4 степени пролапса в зависимости от прогибания створок и наличия нарушений гемодинамики. Первые две степени выявляются чаще всего и характеризуются минимальными изменениями на УЗИ сердца.
Течение пролапса в большинстве случаев благоприятное. Осложнения, такие как митральная недостаточность, инфекционный эндокардит и тяжелые нарушения ритма, возникают очень редко (примерно в 2%).
Лечение должно быть комплексным, продолжительным и индивидуальным. Основные направления терапии:
- Соблюдение распорядка дня и полноценный ночной сон.
- Борьба с хроническими инфекциями (например, санация небных миндалин при хроническом тонзиллите) для предотвращения инфекционного эндокардита.
- Медикаментозная терапия для укрепления организма и нормализации обменных процессов.
- Немедикаментозная терапия, включая психотерапию, аутотренинг, физиотерапию, водные процедуры, рефлексотерапию и массаж.
- Физическая активность. Большинство детей с пролапсом хорошо переносят нагрузки, но следует избегать видов спорта с резкими движениями (прыжки, борьба). Ограничение физической активности необходимо только при нарушении гемодинамики, в этом случае назначаются занятия лечебной физкультурой.
Профилактические осмотры детей и подростков с пролапсом митрального клапана должны проводиться не реже двух раз в год у детского кардиолога.
О предупреждении врожденных пороков сердца
Врожденные пороки сердца, как и другие пороки развития органов, не возникают случайно. Существует около 300 факторов, нарушающих развитие сердца, из которых лишь 5% имеют генетическую природу. Остальные пороки вызваны воздействием внешних и внутренних неблагоприятных факторов на будущую маму. К ним относятся:
- различные виды излучения;
- медикаменты, не предназначенные для беременных;
- инфекционные заболевания, особенно вирусные (например, краснуха);
- контакт с тяжелыми металлами, кислотами и щелочами;
- стрессы;
- употребление алкоголя, курение и наркотики.
Врожденные дефекты сердечной мышцы или сосудов можно выявить уже на 20-й неделе беременности, поэтому всем беременным женщинам рекомендуются плановые ультразвуковые обследования. Определенные УЗИ-признаки могут указывать на сердечные патологии у плода и направить будущую маму на дополнительное обследование в специализированное учреждение. Если диагноз подтверждается, врачи оценивают тяжесть порока и определяют возможное лечение. Малыш с врожденным пороком сердца рождается в специализированном стационаре, где ему сразу оказывают кардиологическую помощь.
Таким образом, профилактика пороков развития, их своевременное выявление и лечение помогут улучшить качество и продолжительность жизни ребенка, а в идеале — предотвратить аномалии сердечно-сосудистой системы. Берегите здоровье!
Автор: врач-кардиолог Мицьо Виктор Петрович
Анатомия порока
В здоровом сердце взрослого человека предсердия полностью изолированы друг от друга. Левое предсердие принимает кровь из легких, обогащенную кислородом, готовую к доставке ко всем органам. В правом предсердии находится венозная кровь с низким содержанием кислорода. При врожденной патологии сердца — дефекте межпредсердной перегородки (ДМПП) — возникает патологическое отверстие, через которое кровь перемещается из левого предсердия в правое.
Какие последствия может иметь такая аномалия? Правая часть сердца перекачивает кровь в легкие для насыщения кислородом. При забросе дополнительного объема крови происходит перегрузка легочных сосудов. Это может привести к сердечной недостаточности и повышению давления в легочной артерии (легочной гипертензии).
Виды ДМПП
Врожденный порок сердца в виде дефекта межпредсердной перегородки имеет несколько разновидностей, различающихся по размеру отверстия:
- Малое отверстие — не влияет на работу сердца и протекает бессимптомно.
- Среднее отверстие чаще выявляется у подростков и взрослых.
- Большое отверстие имеет явные признаки и диагностируется сразу после рождения.
Дефект межпредсердной перегородки классифицируется также по характеру:
- Первичный — может достигать 5 см и возникает из-за недоразвития первичной предсердной перегородки.
- Вторичный — связан с недоразвитием вторичной перегородки и обычно имеет отверстие 1–2 см.
- Полное отсутствие перегородки, известное как трехкамерное сердце, характеризуется двумя желудочками и одним общим предсердием.
По местоположению порок может быть:
- Центральным;
- Верхним;
- Нижним;
- Задним;
- Передним.
Внутриутробный кровоток плода не затрагивает легкие и проходит только через сердце. Проход между предсердиями, называемый овальным окном, необходим для нормального развития плода. После рождения, когда устанавливается кровообращение через легкие, овальное окно закрывается и не считается врожденным пороком сердца.
Изолированный дефект межпредсердной перегородки (ДМПП) занимает второе место по частоте после дефекта межжелудочковой перегородки (ДМПЖ). В сложных пороках его частота достигает 50%. ДМПП часто сопровождается другими пороками развития, такими как заячья губа, врожденные дефекты почек или синдром Дауна.
Симптомы
Симптомы ДМПП зависят от размера отверстия и могут проявляться сразу после рождения или оставаться незаметными до глубокой старости.
Что происходит при большом ДМПП?
У ребенка с таким пороком клиническая картина становится ясной через несколько дней после рождения. Из-за избытка крови в легочной артерии в легких начинается застой жидкости, что приводит к инфицированию и развитию пневмонии. Внешние проявления включают:
- затрудненное дыхание в покое;
- бледную или синюшную кожу;
- учащенное сердцебиение;
- беспокойство.
Такие дети плохо едят и медленно набирают вес. Им необходимо делать глубокие вдохи, из-за чего они часто отвлекаются от еды и давятся грудным молоком.
Детям с большим ДМПП показана операция. Оптимальным временем для нее считается период стабилизации. После первых проявлений порока сосуды сужаются, и наступает временной промежуток, когда симптомы легочной гипертензии исчезают. Ребенок выглядит и чувствует себя здоровым.
При отказе от операции начинается необратимое склерозирование сосудов. Чтобы компенсировать давление, мышечные ткани камер сердца, сосудов и артериол уплотняются и теряют эластичность. Ребенок страдает от артериальной гипоксимии — снижения содержания кислорода в крови.
Средний и малый порок
Средний дефект межпредсердной перегородки проявляется в детстве. Начальные симптомы схожи с признаками большого дефекта и выражаются в сердечной недостаточности, но менее выражены. Дети с этим пороком хуже растут и отстают в развитии от сверстников.
К 3–4 годам могут развиться следующие симптомы:
- частые носовые кровотечения;
- головокружения;
- синюшность кончиков пальцев, носа, ушей и губ;
- обмороки;
- полная непереносимость физической активности;
- сердечные боли;
- учащенное сердцебиение;
- затрудненное дыхание в покое.
С подросткового возраста состояние может ухудшаться из-за нарушений сердечного ритма и утолщения ногтевой фаланги (барабанные палочки). При обследовании могут обнаруживаться увеличение селезенки и печени, тахикардия, хрипы при дыхании, указывающие на застой.
Малый дефект межпредсердной перегородки обычно не проявляется в раннем детстве. Небольшие отверстия могут постепенно закрываться. Если этого не происходит, то в подростковом или взрослом возрасте человек может испытывать слабость, одышку при физических нагрузках и быструю утомляемость.
Поздние проявления ДМПП
Дефект межпредсердной перегородки, если не прооперирован в раннем возрасте, может привести к серьезным осложнениям и угрожать жизни пациента. Наиболее распространенным осложнением является легочная гипертензия, которая вызывает застой жидкости в легких. В редких случаях это может привести к синдрому Эйзенменгера — органическим изменениям в легких. Другие частые осложнения включают:
- сердечную недостаточность, особенно правого предсердия и желудочка;
- нарушения сердечного ритма;
- инсульт.
Без операции продолжительность жизни при этом пороке может сократиться до 35–40 лет.
Причины
По статистике, в педиатрии частота рождения детей с врожденными пороками сердца (ВПС) составляет от 6 до 8 на каждую тысячу новорожденных. Это число увеличивается, если учесть врожденные патологии, не выявленные в младенчестве, которые могут проявиться позже. К ним относятся, например, значительное провисание створок митрального клапана и нарушения в проводящей системе сердца у взрослых.
В нашей стране ежегодно рождается почти 25 тысяч детей с сердечными аномалиями. Благодаря современным технологиям и оборудованию, некоторые из них удается выявить значительно раньше, чем 10-15 лет назад. Причины возникновения врожденных пороков сердца часто остаются неизвестными, однако риск нарушений внутриутробного формирования сердечной трубки могут повышать следующие факторы:
- вирусные инфекции (грипп, краснуха) в первом триместре;
- ожирение, декомпенсированный сахарный диабет, фенилкетонурия у матери;
- злоупотребление алкоголем, курение и употребление наркотиков во время беременности;
- прием некоторых медикаментов (противосудорожные средства, Изотретиноин, Ибупрофен);
- возраст родителей;
- системные болезни соединительной ткани (например, волчанка) у матери;
- контакт с органическими растворителями и ионизирующее излучение на ранних сроках беременности;
- хромосомные аномалии (синдром Дауна, Шерешевского-Тернера).
Родителям важно попытаться понять причину врожденного порока сердца у ребенка. Многие из них винят себя или своих родственников. Наследственная предрасположенность действительно имеет значение, но никто не может точно сказать, как и когда проявятся генетические признаки. Вероятность рождения ребенка с ВПС выше в браках между двоюродными и троюродными родственниками, а также если у родного брата или сестры есть ВПС. В целом этиология врожденных пороков сердца остается недостаточно изученной.
Важно помнить, что родителям ребенка с ВПС не стоит обвинять друг друга. Гораздо важнее разобраться с последствиями и найти оптимальные пути решения проблемы с помощью специалистов.
Диагностика
Если родители замечают у ребенка хотя бы один из указанных симптомов или видят, что он капризен, часто плачет и не хочет играть с другими детьми, им следует обратиться к педиатру. Осмотр, анализ жалоб и сбор анамнеза помогут врачу решить о необходимости дальнейшего обследования. Первые признаки, такие как шумы в сердце, выявляются при аускультации. Последующие обследования включают:
- ультразвуковое исследование сердца (эхокардиография);
- рентген грудной клетки для выявления расширения отделов сердца;
- пульсоксиметрия для определения насыщения крови кислородом;
- катетеризация сердца с контрастом для оценки состояния тканей и структур;
- МРТ – наиболее достоверный метод послойного исследования сердца.
Перед направлением на функциональную диагностику врач назначает биохимический и общий анализ крови.
Лечение
Консервативное лечение ДМПП возможно только при малых и средних пороках. Оно симптоматическое и помогает организму справляться с осложнениями. Назначаемые препараты включают антикоагулянты для уменьшения свертываемости крови и бета-блокаторы или дигоксин для регулирования сердечного ритма. В детском возрасте при малых изолированных пороках врачи ограничиваются наблюдением.
Хирургическое вмешательство — единственный способ устранить дефект межпредсердной перегородки. Врачи рекомендуют проводить операцию в детском возрасте. Существует два метода: щадящий с помощью катетера и операция на открытом сердце. Ранняя операция значительно улучшает качество и продолжительность жизни пациента.
Закрытая операция выполняется через бедренную артерию. Специальная сетка доставляется к перегородке с помощью зонда и перекрывает отверстие. Постепенно оно зарастает собственной тканью. Восстановительный период после эндоваскулярной операции составляет всего несколько дней, и осложнения встречаются редко. Возможные осложнения включают:
- воспаление и инфицирование в месте введения зонда;
- аллергическую реакцию на контрастное вещество для рентгеновского контроля;
- боли в месте введения катетера;
- травму сосуда.
При открытой операции сердце останавливается, и пациент подключается к системе искусственного кровообращения. Заплата на межпредсердную перегородку может быть из ткани перикарда пациента или специального синтетического материала. После операции требуется длительный период реабилитации — не менее месяца. Пациенту необходимо пожизненное наблюдение у кардиолога.
Отказ от хирургического лечения приводит к смерти примерно четверти больных. Прогноз для пациентов, перенесших операцию, благоприятный, большинство из них доживают до старости.
Источник: CardioPlanet.ru
ВПС: общее представление
Под врожденными дефектами педиатрия понимает нарушения строения органов или систем, возникающие внутриутробно. За 40 недель плод проходит все стадии развития — от зиготы до маленького человечка, почти точной копии родителей. Во время беременности формируются все внутренние системы плода, которые должны развиваться по программе, заложенной природой. Если все идет по плану, на 37—41-й неделе малыш появляется на свет с полностью сформированными органами.
Однако иногда система дает сбой. В какой-то момент происходит поломка, и орган перестает развиваться по заданному плану. Это может случиться с любым внутренним органом, но нас интересует сердце. Наиболее уязвимым оно является в период с 2-й по 8-ю неделю после зачатия. В это время женщина часто не знает о новой жизни внутри нее. Любое негативное влияние может оказаться фатальным и спровоцировать появление врожденных пороков сердца (ВПС).
Почему появляются дефекты
Причины пороков у плода остаются неизвестными, но можно выделить несколько факторов, которые могут на них влиять:
-
Хромосомные аномалии. Это структурные или количественные изменения генного материала. Дефект может возникнуть как в материнской, так и в отцовской клетке. Возможны как наследственные изъяны, так и новые мутации. Даже если родители здоровы, иногда дефект может возникнуть в одной половой клетке, что приведет к нарушению, если именно эта клетка станет основой зародыша.
-
Влияние внешних тератогенов. Постоянный контакт с токсинами, особенно в первом триместре, может быть опасен. Например, у женщин, работающих на лакокрасочном производстве, чаще выявляются врожденные пороки сердца (ВПС) на УЗИ. Прием некоторых медикаментов в первом триместре (например, противоэпилептических средств, Ибупрофена, препаратов лития) также может привести к подобным последствиям. Опасны избыток витамина A, ионизирующая радиация и проживание в экологически неблагоприятных районах.
-
Внутриутробные инфекции. Краснуха, особенно при первичном заражении, может вызывать дефекты сердца, поражение глаз и слуха у плода. В первом триместре беременности опасны также грипп и цитомегаловирус, а любое вирусное заражение с лихорадкой представляет риск.
-
Материнские факторы. Риск развития ВПС у детей выше при отягощенном акушерском анамнезе. Выкидыши, особенно на 13-24 неделях, могут указывать на недиагностированный порок. Прием алкоголя и курение матерью также увеличивают риск. Вероятность рождения ребенка с ВПС выше у женщин старше 35 лет и при наличии сахарного диабета.
-
Семейные факторы. Употребление наркотиков (кокаина, марихуаны) отцом младенца также повышает риск развития ВПС.
Хотя важно знать причины и последствия пороков сердца у новорожденных и плодов, часто невозможно однозначно определить, какой фактор стал решающим. Нельзя точно сказать, стала ли причиной дефекта таблетка Ибупрофена, принятая матерью от головной боли, или вирус, который она подхватила. Мы можем лишь предполагать и стараться исключить все негативные факторы.
Многоликость пороков сердца: классификация и виды
Интересна клиническая классификация врожденных пороков сердца (ВПС):
- Цианозные (сопровождаются синюшностью кожи и слизистых). К ним относятся тетрада Фалло, общий артериальный ствол, транспозиция магистральных артерий.
- Сопровождающиеся бледностью (характерно сужение сосудов в коже и слизистых). Это наблюдается при открытом артериальном протоке, дефектах перегородок между желудочками и предсердиями, клапанном стенозе легочного ствола.
- Приводящие к системной гипоперфузии (ослабленному кровотоку). Это характерно для дефектов аорты, таких как стеноз или коарктация.
Еще одна система делит ВПС по особенностям гемодинамики — току крови по сосудам. Важно выделить следующие варианты:
- Связанные с фетальными коммуникациями (особенности кровотока у плода). Движение крови по большому кругу зависит от проходимости открытого артериального протока (ОАП).
- Не связанные с сохранением фетальных структур.
Первый случай критичен для новорожденного. Кровообращение зависит от того, как долго сохраняются открытое овальное окно и ОАП. Они должны закрываться в процессе рождения, чтобы обеспечить переход к новому режиму кровообращения с двумя кругами. При этом типе ВПС кровеносная система функционирует только при наличии фетальных структур — открытого овального окна или артериального протока. Если они закрываются, возникает критическая ситуация и сердечная недостаточность.
Симптомы и признаки ВПС
Порок сердца у новорожденных проявляется по-разному. Клиническая картина зависит от типа дефекта, степени нарушения гемодинамики и наличия сопутствующей патологии. Некоторые врожденные пороки сердца (ВПС) остаются бессимптомными и не выявляются в период новорожденности, а диагностируются позже, в возрасте 1—6 месяцев. Реже ВПС обнаруживаются после первого года жизни.
Основные симптомы врожденной патологии сердца:
- цианоз или бледность кожи и слизистых оболочек;
- кардиальные шумы;
- признаки сердечной недостаточности.
В течение заболевания у новорожденных выделяют два критических периода:
- 3—5-й день: закрытие овального окна;
- 3—6 недель: снижение сосудистого легочного сопротивления.
В эти периоды нарушается гемодинамика, что ухудшает состояние ребенка.
У грудничков и детей младше 3 лет о наличии ВПС могут свидетельствовать такие симптомы:
- синюшность или бледность кожи;
- быстрая утомляемость при кормлении;
- одышка;
- дефицит веса;
- отставание в физическом развитии;
- частые заболевания бронхов и легких.
Некоторые пороки сердца остаются недиагностированными до подросткового возраста. Заподозрить патологию можно по следующим признакам:
- отставание в физическом развитии (низкий вес и рост);
- быстрая утомляемость, слабость;
- учащенное сердцебиение;
- отеки конечностей;
- бледность или цианоз кожи;
- повышенная потливость;
- кардиовокальный синдром (осиплость голоса, стридор – свистящее шумное дыхание).
Если подросток демонстрирует эти симптомы, необходимо обратиться к врачу для выяснения причины и исключения врожденного порока сердца.
Схема диагностики
Как обследовать ребенка при подозрении на врожденные пороки сердца? Схема диагностики включает следующие этапы:
- Физикальный осмотр. Оценивается общее состояние ребенка, пульс и частота дыхания. Особое внимание уделяется цвету кожных покровов и слизистых оболочек для выявления бледности или цианоза. Проводится аускультация сердца и легких.
- Инструментальные исследования. При выявлении отклонений на этапе физикального осмотра необходимо дополнительное обследование для определения порока сердца, его разновидности и степени нарушения гемодинамики.
Аускультация сердца — важный этап первичной диагностики врожденных пороков. Оценку сердечных тонов проводит неонатолог в родильном доме или педиатр на приеме. Следует учитывать, что сердечные шумы обнаруживаются у 60—70 % новорожденных в первую неделю жизни, но это не всегда указывает на патологию. Часто шумы связаны с перестройкой кровообращения и являются вариантом нормы.
Шумы, вызванные нарушениями гемодинамики при ВПС, обычно выявляются на 4—5-й день жизни или позже. Особое внимание следует уделить шумам, сохраняющимся более 3 дней и сопровождающимся признаками сердечной недостаточности:
- одышка;
- учащенное сердцебиение и дыхание;
- отеки конечностей;
- увеличение печени;
- усиленная потливость;
- снижение диуреза;
- слабое сосание груди (у новорожденных и детей до года).
Отсутствие сердечного шума не исключает порока. При наличии других симптомов патологии необходимо провести обследование.
При выявлении патологических шумов или других признаков ВПС ребенок направляется к кардиологу для дальнейшего обследования:
- Электрокардиография (ЭКГ). Оценка основных показателей работы сердца.
- ЭхоКГ. Ультразвуковое исследование сердца, позволяющее выявить дефекты развития и оценить ток крови.
- Пульсоксиметрия. Оценка степени насыщения крови кислородом и выявление гипоксии.
- Рентгенография грудной клетки. Оценка размеров сердца и состояния легочного рисунка, что помогает в диагностике многих ВПС.
- Компьютерная томография. Получение подробного изображения камер сердца и близлежащих сосудов. В качестве альтернативы рассматривается МРТ.
- Катетеризация сердца. Проводится после полного эхографического обследования и дает более детальную информацию о работе органа.
Неонатальный скрининг
Согласно протоколу, всем новорожденным рекомендуется проводить пульсоксиметрию в родильном доме или в отделении патологии новорожденных, если младенец был госпитализирован. Тест выполняется в первые 24—48 часов жизни и позволяет выявить недиагностированные внутриутробные пороки, включая критические (врожденные пороки сердца, угрожающие жизни ребенка). Также допускается проведение теста в первые сутки после рождения при ухудшении состояния малыша.
Пульсоксиметрию проводит медсестра отделения новорожденных. Оценивается степень насыщения кислородом (SaO2) на правой руке и ноге. Результаты теста анализирует врач:
- Отрицательный тест — SaO2 более 95 % на обеих конечностях; разница между показателями на руке и ноге не более 3 %. Это хороший результат, указывающий на отсутствие нарушений кровотока.
- Положительный тест — SaO2 менее 95 % на одной конечности и 90—95 % на другой или менее 90 % на обеих конечностях; разница более 3 %. Это неблагоприятный результат, требующий консультации кардиолога и дополнительного обследования.
Золотым стандартом диагностики врожденных пороков сердца считается эхоКГ. Полный объем обследования определяет лечащий врач с учетом конкретной клинической ситуации.
Методы лечения пороков
Принцип лечения определяется индивидуально. Мы учитываем протоколы и рекомендации, а также разрабатываем тактику ведения пациента с учетом типа порока, состояния кровотока и других параметров.
Принимают ли лекарства
Нельзя устранить анатомический дефект с помощью таблеток или уколов. Мы назначаем медикаменты ребенку только на этапе подготовки к операции. Используются препараты из различных групп:
- гликозидные сердечные средства;
- АПФ-ингибиторы;
- блокаторы кальциевых каналов;
- антагонисты рецепторов к альдостерону;
- вазодилататоры;
- диуретики.
Цели лечения — компенсировать сердечную недостаточность и облегчить состояние пациента. В некоторых случаях медикаментозная терапия продолжается и после операции, особенно если вмешательство не было радикальным.
В дополнение к основной терапии назначаются витамины. Также показана санация очагов хронической инфекции для профилактики бактериальных осложнений. При недостаточности кровообращения проводится оксигенотерапия для насыщения крови кислородом.
Хирургия и показания к ней
Операция необходима в следующих случаях:
- критический ВПС у новорожденного;
- признаки острой застойной кардионедостаточности;
- сильная легочная гипертензия (повышение давления в легочных сосудах);
- значительное снижение кислородного насыщения тканей;
- нарушение работы клапанов сердца;
- выраженная задержка физического развития;
- дисфункция других органов на фоне порока сердца.
Варианты хирургического вмешательства:
- Радикальная операция — полная анатомическая коррекция порока и устранение аномалий развития.
- Коррекция гемодинамики — разделение венозного и артериального кровотока. Применяется, если полное восстановление целостности сердца невозможно.
- Паллиативная операция — вмешательство, не исправляющее дефект, но временно улучшающее кровоток и предотвращающее осложнения. Часто служит подготовительным этапом к радикальной или гемодинамической операции.
Таблица ниже содержит объемы и сроки хирургического лечения распространенных пороков.
Хирургическое лечение может быть выполнено в двух вариантах:
- Закрытая операция. Включает эндоваскулярное вмешательство, при котором манипуляции проводятся без разрезов через сосуды. Наркоз не требуется, достаточно местной анестезии. Также к закрытым операциям относятся вмешательства с вскрытием грудной клетки без доступа к сердечным камерам.
- Открытая операция. Проходит в условиях искусственного кровообращения с вскрытием камер сердца. Здесь выполняются все сложные реконструктивные вмешательства.
Последствия: что будет, если не лечить?
Врожденный дефект сердца требует обязательного лечения. Без него возможны серьезные осложнения:
- сердечная недостаточность — состояние, при котором сердце не справляется с функциями;
- нарушение ритма;
- инфекционный эндокардит — бактериальное поражение сердечных клапанов;
- бронхолегочные заболевания (бронхит, пневмония).
Эти состояния значительно ухудшают качество жизни, мешают нормальному развитию и могут привести к инвалидности.
Профилактика
Можно ли предупредить болезнь? Точные причины пороков развития сердца неизвестны, и мы не можем полностью контролировать этот процесс. Однако мы можем выявить патологию на этапе внутриутробного развития, оценить возможные риски и подготовиться к рождению ребенка с пороком. Если дефект несовместим с жизнью, рекомендуется прерывание беременности до 22 недель.
Источник: cardiograf.com
Виды пороков
Все врожденные пороки сердца (ВПС) классифицируются по патофизиологическому принципу в зависимости от гемодинамических нарушений в обоих кругах кровообращения. Описано более 140 вариантов ВПС, встречающихся с различной частотой в популяции.
Классификация ВПС учитывает клинические симптомы, связанные с анатомическими нарушениями. Важны особенности сброса крови между правой и левой сторонами сердца и в главные сосуды, а также наличие аномалий клапанного аппарата и аортального ствола. Гемодинамические нарушения могут вызывать цианоз — синеватую окраску кожи и слизистых из-за недостатка кислорода в тканях.
Общепринятая классификация ВПС среди врачей выглядит следующим образом:
| ТИП ГЕМОДИНАМИЧЕСКОГО НАРУШЕНИЯ | БЕЗ ПРИЗНАКОВ ЦИАНОЗА | С ОБЯЗАТЕЛЬНЫМ ЦИАНОЗОМ |
|---|---|---|
| Синдром переполнения малого круга кровообращения (сбрасывание крови с левых отделов в правые) | Открытый артериальный проток, дефекты перегородок между желудочками или предсердиями, предсердно-желудочковая коммуникация | Синдром Эйзенменгера (дефект межжелудочковой перегородки, правостороннее расположение аорты, гипертрофия миокарда правого желудочка), общий артериальный ствол, транспозиция основных сосудов |
| Синдром обеднения малого круга (сбрасывание крови с правых отделов в левую часть сердца) | Изолированный стеноз части легочной артерии | Болезнь Фалло (дефект межжелудочковой перегородки, правостороннее расположение ствола аорты, заращение легочной артерии, гипертрофия миокарда правого желудочка), полное заращение створок трикуспидального клапана |
| Синдром обеднения большого круга кровообращения | Сужение просвета в сегменте аорты (коарктация) | |
| Без нарушений кровотока | Истинное или ложное смещение сердца вправо (декстрокардия), аномалии расположения аортальной дуги и ее ветвей, незначительное отверстие в мышечной части межжелудочковой перегородки |
Клинические проявления
Признаки врожденных пороков сердца (ВПС) в двух третях случаев не проявляются сразу после рождения. Лишь в одной трети случаев состояние детей может быть тяжелым: они синюшны, страдают от одышки, отказываются от еды и постоянно плачут. В большинстве случаев история болезни начинается значительно позже новорожденности. Клиника ВПС разнообразна и зависит от структурных особенностей порока, степени его компенсации и возможных осложнений. Выделяют три фазы:
-
Адаптация организма к нарушениям кровообращения. Компенсация порока зависит от тяжести нарушений. При незначительных пороках симптомы слабо выражены, а при крупных дефектах может развиться гипертрофия миокарда, переходящая в декомпенсацию.
-
Фаза относительного благополучия наступает примерно через три года. Этот период характеризуется уменьшением жалоб, улучшением состояния ребенка, повышением физической активности и уровня развития. Чем лучше дети компенсируют гемодинамические и газообменные нарушения, тем заметнее улучшение.
-
Декомпенсация — заключительная стадия, сопровождающаяся хронической сердечно-сосудистой недостаточностью. Она возникает после истощения компенсаторных возможностей организма и приводит к дегенеративно-дистрофическим процессам во внутренних органах. Различные инфекции и сопутствующие болезни могут ускорить наступление этой стадии.
В стадии декомпенсации дети жалуются на боли в области сердца, слабость и нехватку воздуха даже при минимальной физической нагрузке. Степень цианоза зависит от вида порока. Его появление часто сопровождается признаками сгущения крови: полицитемией (увеличение количества красных кровяных телец) и гипергемоглобинемией (повышенный уровень гемоглобина). Признаки хронической сердечной недостаточности у детей с ВПС включают отставание в физическом развитии, постоянную слабость, бледность, синеватый оттенок кожи, отеки на ногах, а также изменения формы ногтей и фаланг.
Как диагностировать
Хотя врожденные и приобретенные пороки сердца различаются по причинам и времени появления первых симптомов, иногда требуется их дифференциация. В этом случае полезны данные анамнеза, например, информация о перенесенной ангине.
Диагностика врожденных пороков сердца (ВПС) начинается еще в пренатальный период. В стандарт обследования будущих матерей входит УЗИ сердца плода после 14-й недели гестации. При подозрении на ВПС рассматриваются дополнительные обследования. Роды проводятся в медицинском учреждении, где возможно выполнение операции сразу или вскоре после рождения.
Коррекция пороков сердца у плода — это перспективное направление фетальной хирургии, развитой в США и других странах с высокоразвитыми медицинскими системами. В России некоторые крупные медицинские центры проводят такие операции, но не в полном объеме.
К сожалению, не всегда удается выявить ВПС до рождения. Обследование детей раннего возраста включает:
- Сбор анамнеза, внешний осмотр педиатра или детского кардиолога, аускультацию (выслушивание сердечных тонов и шумов).
- ЭКГ (электрокардиограмма) — традиционный метод, показывающий перегрузку отделов сердца и наличие нарушений ритма.
- Эхокардиография — ультразвуковое исследование сердца и сосудов, наиболее информативный метод, позволяющий поставить точный диагноз в любом возрасте и выявить структурные изменения и состояние кровотока.
- Рентгеновские методы — оценивают расположение и размеры сердца, состояние легочных сосудов, служат дополнительным способом диагностики при подозрении на ВПС.
Не обязательно использовать все эти методы для определения врожденного порока сердца. В некоторых сомнительных случаях могут быть назначены инвазивные вмешательства:
- Зондирование сердца — с помощью катетера измеряется давление в камерах, берутся пробы крови для определения насыщения кислородом, вводится контраст для снимков.
- Ангиокардиография — исследование с контрастом, позволяющее получить точную анатомическую картину полостей сердца, легочного кровообращения и магистральных сосудов, используется для получения полной информации перед операцией.
Как лечить
Проведенное обследование помогает определить тактику дальнейшего ведения пациента. Возможны три варианта:
- срочная операция;
- плановое хирургическое лечение;
- поддерживающая терапия без операции.
В настоящее время диагноз ВПС не влияет на продолжительность и качество жизни, если ребенку своевременно оказывается квалифицированная медицинская, в том числе хирургическая, помощь.
Оперативное лечение врожденных пороков сердца проводится, когда консервативные методы не могут стабилизировать состояние пациента. В зависимости от типа аномалии и тяжести клинических проявлений операции делятся на три категории:
- экстренные – проводятся немедленно после постановки диагноза, чаще всего при критическом состоянии новорожденных;
- неотложные – подготовка ребенка занимает несколько дней;
- плановые – выполняются в удобное для пациента и врача время, обычно в возрасте от 3 до 12 лет.
По подходу к хирургическому лечению операции бывают двух видов:
- Радикальные вмешательства – полное устранение порока, возможно при хорошо сформированных отделах сердца и разделении кругов кровообращения с сохранением нормальной анатомии.
- Паллиативные вмешательства – проводятся при сложных пороках для облегчения состояния пациента, могут быть как самостоятельными, так и подготовительными к радикальному вмешательству.
По технике выполнения операции различают:
- открытые – проводятся через разрез в грудной клетке на работающем или остановленном сердце с использованием аппарата искусственного кровообращения;
- рентгенохирургические – под контролем рентгена вводятся катетеры с баллончиками для расширения суженных участков и создания заплат в перегородках сердца.
Со временем ребенку может потребоваться повторная операция, если по мере роста организма произойдет разрушение искусственного клапана или протеза. В будущем проблему могут решить материалы, выстланные изнутри собственными клетками пациента. Отказ в операции получают только пациенты с тяжелой сердечной недостаточностью (сложные дефекты развития, кардиомиопатия, распространенная опухоль).
Профилактика врожденных пороков сердца включает планирование беременности в оптимальный период для женщины, генетическое обследование и консультирование пар, в которых уже есть больной ребенок, здоровый образ жизни, вакцинацию от краснухи и гриппа, контроль уровня сахара при диабете и прием витаминных комплексов по назначению врача.
Источник: SilaSerdca.ru