1
- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Возникновение аутотрофных организмов в ходе эволюции жизни на Земле и появление кислорода как окислителя предоставили потребителям возможность более эффективно извлекать энергию из органических веществ, что способствовало развитию аэробных организмов. Аэробное окисление обеспечивает больший энергетический выход на единицу массы органического субстрата. Появление многоклеточных организмов создало проблему доставки кислорода во все клетки. Эволюционно возникли специальные молекулы-переносчики кислорода, среди которых у позвоночных ключевую роль играет гемоглобин. Он увеличивает способность крови переносить кислород в 50 раз и участвует в транспортировке углекислого газа и ионов водорода [13, 21, 27].
Гемоглобин (от греч. haemo – кровь и лат. globus – шар) — красный железосодержащий ферропротеин, дыхательный пигмент крови человека и некоторых животных. Он относится к сложным белкам — хромопротеидам [21].
В организме гемоглобин выполняет следующие функции:
-
Транспортно-дыхательная:
- перенос кислорода от альвеол к периферическим тканям;
- транспорт углекислого газа и катионов водорода от тканей к легким для выведения.
-
Буферная функция — поддержание кислотно-основного баланса крови. Гемоглобиновая буферная система сохраняет рН крови в нормальном диапазоне и составляет около 75 % от общей буферной емкости [13, 21].
Молекула гемоглобина состоит из белковой части — глобина и небелковой — гема. Гем — тетрапиррольная структура протопорфирина IX, содержащая ион Fe2+. Он является простетической группой ферропротеинов (гемоглобина, миоглобина, цитохромов и др.) и обеспечивает их функции: связывание и транспорт кислорода (гемоглобин), участие в цепи переноса электронов (цитохромы) и разложение перекисей (каталаза и пероксидаза) [18, 21].
Гемоглобины — мультимерные белки. Основные типы гемоглобина имеют структурное сходство: все они — тетрамеры, состоящие из двух пар протомеров: пары идентичных субъединиц α-цепей и другой пары. Комплекс из одного гема и одной полипептидной цепи называется Сведберговой единицей. Таким образом, молекула гемоглобина состоит из четырех Сведберговых единиц [5, 18, 21].
Известно более 300 генетически обусловленных типов гемоглобина. Номенклатура была принята на Х Международном гематологическом конгрессе в Стокгольме в 1964 году. Типы гемоглобина обозначаются буквами латинского алфавита от A до G и S [6].
К наиболее значимым изотипам гемоглобина человека относятся:
- Гемоглобин взрослого — HbA (от лат. adults — взрослый), включает более сотни подтипов, основные из которых HbA1 и HbA2.
- Фетальный гемоглобин — HbF (от лат. fetus — плод).
- Эмбриональный гемоглобин — HbP (от греч. embryon — зародыш).
У человека и высших животных гемоглобин всех типов является тетрамером, состоящим из четырех субъединиц-протомеров [6, 11].
Фетальный и эмбриональный гемоглобины — стадиоспецифические белки, некоторые авторы объединяют их термином антенатальные гемоглобины [7, 17].
Примитивный гемоглобин P (HbP) обладает более высоким сродством к кислороду, чем HbA1. Его синтез активируется в раннем эмбриогенезе и происходит в желточном мешке. HbP присутствует в эритроцитах эмбриона с 4-й по 18-ю неделю гестации, особенно между 5-й и 12-й неделями [6, 21].
HbP имеет несколько подтипов, среди которых Gower-I, Gower-II и Hb-Portland. Все они являются тетрамерами, различающимися структурой одной из двух пар полипептидных цепей: Gower-I — ε4; Gower-II — α2ε2; Hb-Portland — ζ2γ2 [5, 11, 13, 20].
Эмбриональный гемоглобин по физико-химическим свойствам схож с фетальным, имеет близкие параметры по спектру поглощения и коэффициенту седиментации — 4,5 S, но меньшую электрофоретическую подвижность [6, 18, 21].
Фетальный гемоглобин — тетрамер, состоящий из двух α- и двух γ-протомеров. В γ-цепи содержится меньше валина, пролина и гистидина, но больше изолейцина, серина и треонина. Общее количество аминокислот в γ-цепи равно 146 [5, 18, 20].
Смена различных типов гемоглобина в процессе онтогенеза обусловлена функциональными и физико-химическими особенностями каждого изотипа, что обеспечивает адаптацию в разных условиях организма. В первые недели эмбрионального развития активируется синтез гемоглобинов типа HbP. К концу 12-й недели продукция ε-цепи эмбрионального гемоглобина полностью прекращается, и с 12-й по 24-ю неделю почти весь гемоглобин плода представлен α- и γ-протомерами, т.е. фетальным гемоглобином. HbF обнаруживается у эмбрионов на ранних сроках гестации, но его уровень значительно ниже, чем у HbP [4, 10, 12].
После рождения уровень HbF в крови уменьшается примерно на 3 % в неделю и к шестому месяцу жизни составляет менее 2–3 % общего количества гемоглобина, заменяясь на гемоглобин взрослого (HbA1). Синтез HbP в постнатальном периоде у здорового человека полностью ингибирован [10, 12].
Изоэлектрическая точка фетального гемоглобина составляет 6,9–7,15 [13, 21].
HbF, как и HbP, устойчив к денатурирующему воздействию щелочей, что используется при его клиническом определении [5, 6, 21].
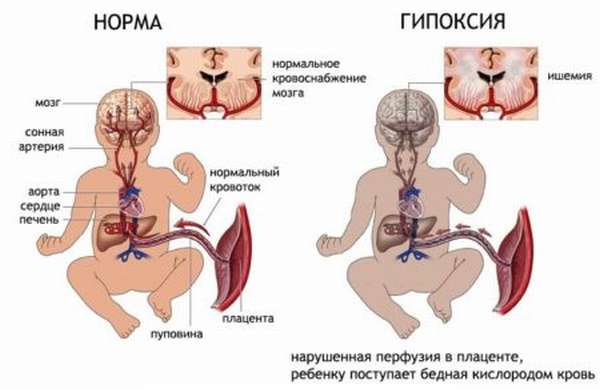
Антенатальные гемоглобины имеют большее сродство к кислороду, что позволяет эритроцитам эмбриона и плода поглощать и отдавать кислород при более низком парциальном давлении. Осмолярность кислорода в крови плода примерно в 2 раза ниже, чем у взрослого, но высокая тропность HbF к кислороду обеспечивает адекватную оксигенацию тканей плода в условиях физиологической гипоксии. Эритроциты с HbF также более устойчивы к гемолизу [2, 23, 30].
Количественный анализ антенатальных гемоглобинов в крови имеет важное значение в клинической практике.
Исследования показывают, что уровень фетального гемоглобина значительно повышается у взрослых с гомозиготной формой β-талассемии и серповидноклеточной анемией, где уровень HbF превышает норму на 30 %. Также отмечается повышение HbF у недоношенных детей и при различных гематологических заболеваниях, острых и хронических интоксикациях, эндокринных нарушениях и сердечно-сосудистой патологии [3, 9, 28].
Рост концентрации HbF у беременных женщин является тревожным признаком, указывающим на развитие осложнений, таких как гестозы и угроза прерывания беременности [1, 22].
У людей, живущих в условиях хронической гипоксии, например, в высокогорье или на Крайнем Севере, наблюдается компенсаторное повышение HbF, причем его накопление превышает образование других изотипов [25, 26].
Недавние данные показывают, что повышение уровня HbF связано с онкогематологическими заболеваниями, такими как миелопролиферативные заболевания (эритремия, сублейкемический миелоз, острый и хронический лимфолейкоз), что подчеркивает его клинико-диагностическую значимость как канцероэмбрионального антигена [15, 19].
Снижение уровня HbF наблюдается при железодефицитной, В12 (фолиево)-дефицитной, гемолитической и постгеморрагической анемиях, а также у детей с гемолитической болезнью и задержкой внутриутробного развития [24, 29].
У взрослых снижение HbF фиксируется при тромбоцитопенической пурпуре, лейкозе и сфероцитарной гемолитической анемии [3, 18].
Сведения о клинико-диагностическом значении эмбрионального гемоглобина ограничены, так как его гены полностью репрессированы у детей и взрослых. Кроме того, сложности получения и очистки HbP затрудняют его изучение [18, 21].
Тем не менее, в последние годы появились работы, подтверждающие роль этого протеина как канцероэмбрионального антигена, особенно при хронических миелопролиферативных заболеваниях [15, 19].
Библиографическая ссылка
Расшифровка понятия фетальный гемоглобин
Фетальный гемоглобин — это форма гемоглобина, которая обеспечивает правильное насыщение организма кислородом. Он образуется в эритроцитах эмбриона и часто называется плодным гемоглобином.
Гемоглобин F имеет следующую схему развития:
- Появляется у эмбриона на 9-10 неделе беременности.
- К концу первого триместра является основным видом гемоглобина у будущего ребенка.
- Сохраняется у новорожденного.
- Резко снижается с 25 дня жизни.
- В период с 25 по 105 день жизни уровень гемоглобина F снижается до нормы, характерной для взрослых.
Важно! Безопасный уровень фетального гемоглобина у взрослого не должен превышать одного процента от общего количества гемоглобина. Основным становится гемоглобин A, который заменяет фетальный и обеспечивает организм необходимым количеством кислорода.
Важность фетального гемоглобина для новорожденного
Данное белковое соединение обладает высоким сродством к кислороду, что позволяет эффективно извлекать кислород из гемоглобина беременной женщины и передавать его ребенку через плаценту. После рождения это сродство становится излишним, так как фетальный гемоглобин (HbF) хуже делится кислородом с тканями. Это может стать решающим фактором при сердечной или легочной гипоксемии. Чтобы избежать подобных проблем, фетальный гемоглобин начинает заменяться более функциональным гемоглобином-А еще до рождения.
Резкий скачок парциального давления кислорода в артериальной крови (раО2) с 25-32 мм рт. ст. у плода до 87-98 мм у новорожденного приводит к недостаточному синтезу эритроцитов в первые 6-9 недель жизни. Это негативно сказывается на костномозговом кроветворении и может вызвать физиологическую анемию. В группу риска попадают недоношенные дети, у которых после рождения быстро увеличивается масса тела и объем крови.
Снижение количества гемоглобина уменьшает парциальное давление кислорода в тканях, что приводит к повышению уровня эритропоэтина и увеличению продукции эритроцитов.
Польза эмбрионального гемоглобина
Это белковое соединение важно не только для плода и новорожденного, но и для диагностики различных заболеваний. Оно применяется в следующих анализах:
- Для проверки степени созревания ребенка при недоношенности.
- Для подтверждения или опровержения гемолитической анемии у грудничков. При этой патологии проводятся переливания крови, и их эффективность оценивается по уровню данного соединения.
- Для обнаружения лейкоза, который характеризуется повышенным уровнем фетального гемоглобина.
- Для выявления предрасположенности к гипоксии и гипоксемии. При наличии этих состояний уровень белка значительно выше нормы.
При проблемах с кислородным насыщением гемоглобин-А может быть заменен белком типа f, так как первый не может эффективно обеспечивать органы кислородом в таких условиях.
Отличия между белковыми соединениями А и F
Главное различие между двумя типами белка — это способность насыщать тело кислородом. Белок типа F выполняет эту функцию лучше, чем белок типа A. Это связано с несколькими факторами:
- Различия в полипептидной цепи.
- Необходимостью плода получать кислород из внутриутробной водной среды, где его содержание значительно ниже, чем в воздухе, который он вдыхает после рождения.
- Меньшим объемом крови, необходимым для транспортировки кислорода к органам и системам организма.
Недостатки белка типа F:
- Невозможность выдерживать изменения температуры.
- Длительная и сложная адаптация к изменению кислотности окружающей среды.
У ребенка с предрасположенностью к легочным патологиям повышенная отдача кислорода гемоглобином F может вызвать гипоксию.
Что собой представляет эмбриональный гемобелок
В медицине сложный белок, известный как гемоглобин hbf или f, формируется у эмбриона на 9-13 неделе. Его основная функция — извлечение кислорода из крови, поступающей через плаценту от матери, и распределение кислорода по органам и тканям плода. После рождения он заменяется гемоглобином А, который присутствует в крови взрослого человека.
На ранних стадиях развития эмбриона в его крови также присутствует другой вид гемоглобина — Р, называемый «примитивным». Он обладает высокой устойчивостью к щелочной среде.
Строение эмбрионального гемобелка и синтез в человеческом организме
Белок, обнаруживаемый у трехмесячного эмбриона, состоит из двух цепочек α и двух цепочек γ (α2γ2). В крови взрослого человека он присутствует в количестве менее 1-7% от общего содержания эритроцитов, тогда как у плода эта форма является основной. Это соединение имеет низкую стойкость к температурным колебаниям и реагирует на внешние раздражители.
По своей структуре молекулы больше напоминают кислородные, что обеспечивает эффективный газообмен, несмотря на небольшой объем прокачиваемой крови. В γ-цепи лизин заменяет серин, что повышает кислородную активность молекул.
Выработка гемоглобина f начинается с замещения. Первичный гемобелок Р вытесняет примитивные форменные структуры кровяных клеток, трансформируется и становится более устойчивым к щелочной среде. Биохимический анализ выявляет различия в 39 позициях. Во время беременности эти изменения могут восприниматься как временное ухудшение состояния, особенно в начале второго триместра, который считается одним из самых нестабильных периодов.
С 8-й по 24-ю недели внутриутробного развития содержание hbf составляет 98%, а после 24-й недели — 90%. В предродовой подготовке организма матери его количество постепенно уменьшается, а после родов у новорожденных уровень hbf колеблется между 70-85% от общего содержания гемоглобинов.
К концу первого года жизни уровень hbf снижается до 1,5%. В этот период структурное сходство с кислородной молекулой становится опасным, так как гемобелок имеет повышенную восприимчивость к кислороду, что может замедлять снабжение тканей. Даже при незначительных патологиях дыхательной системы может развиваться гипоксия. Поэтому к полутора годам практически весь эмбриональный гемоглобин заменяется типами А, А1 и А2.
Отличия эмбрионального и взрослого гемобелка
Форменные фракции крови различаются аббревиатурами и структурой полипептидных цепочек, но их основная функция — газообмен — остается аналогичной. Различия в конструкции объясняются условиями существования организмов: эмбриональный гемоглобин извлекает кислород из водной среды, и его содержание в крови, проходящей через плаценту, ниже, чем в крови, циркулирующей по сосудам.
У беременных женщин формируется плацентарный кровоток, однако объем воздуха, попадающего в легкие, остается таким же, как и в обычном состоянии. Поэтому необходимо особое соединение, которое позволяет эффективно усваивать кислород и доставлять его к плоду.
В крови здорового человека в возрасте 25-45 лет циркулирует 97-98% гемоглобина А1, до 5% — А2 и менее 1% — А3. Структурные единицы клеток крови незначительно изменяются при температурных колебаниях, выдерживают изменения давления и быстро адаптируются к колебаниям кислотности. Если бы гемоглобин взрослых трансформировался под воздействием внешних факторов и реагировал на них как f-форма, то после болезней восстанавливались бы лишь единицы.
Полезные свойства эмбрионального гемоглобина
Анализы на гемоглобин F помогают выявить патологии на ранних стадиях. Исследования назначают:
- для проверки физиологического развития недоношенных новорожденных;
- для раннего обнаружения лейкоза;
- для подтверждения или опровержения диагноза гемолитической анемии у младенцев до 5 месяцев;
- для предупреждения апноэ;
- для выявления предрасположенности к гипоксии.
Увеличенное количество гемоглобина Hbf указывает на талассемию, предрасположенность к заболеваниям дыхательной системы, анемия различного типа, а также на возможность развития лейкоза и нарушений распределения кислорода в организме. Определить причину изменения значений можно только после тщательного обследования. Младенцев с отклонениями обычно ставят на учет.
Источник: krovinfo.com
Строение фетального гемоглобина
Соединение типа F — это белок, представляющий собой гетеротетрамер, состоящий из двух α-цепей и двух γ-цепей. В организме взрослого человека его содержание невелико — до 1% от общего объема.
При анализе этот белок определяется в 7% эритроцитов. У плода фетальный гемоглобин преобладает.
Гемоглобин F обладает повышенным сродством к кислороду, что позволяет эффективно снабжать организм кислородом при небольшом объеме крови плода. Однако этот белок имеет низкую стойкость к разрушению и нестабилен при изменении pH и температуры. В последние недели беременности и в первые недели жизни у новорожденного происходит замена гемоглобина F на гемоглобин взрослого человека. Этот процесс сопровождается увеличением объема крови. Гемоглобин взрослого менее активен по отношению к кислороду, но более устойчив к денатурации при изменениях pH и температуры. Замещение происходит из-за снижения уровня синтеза γ-цепей и одновременного увеличения синтеза β-цепей в эритроцитах.
Повышенное сродство к кислороду у белка типа F связано с особенностями его первичной структуры. В γ-цепи лизин-143 заменен на серин-143, который имеет отрицательный заряд. Это приводит к снижению положительного заряда молекулы HbF, что увеличивает ее активность в отношении кислорода.
Синтез в организме человека
Белковая структура HbF начинает формироваться на 12-14 неделе развития плода, когда эмбриональный белок заменяется на белок типа F. Первичная структура HbF отличается от HbA в 39 позициях. Уникальные свойства HbF обеспечивают его устойчивость к щелочной среде, что стало основой для методики определения этого гемоглобина в организме. Кроме того, фетальный гемоглобин может трансформироваться в метгемоглобин, обладающий специфическим спектром поглощения в ультрафиолете.
При рождении до 85% общего количества гемоглобина составляет HbF. В течение первого года жизни продукция этого белка замедляется, и к третьему году его уровень становится сопоставим с уровнем у детей, достигая 1-1,5%. После рождения повышенное сродство HbF к кислороду может быть вредным, особенно при легочных или сердечных заболеваниях, так как это может привести к гипоксии. Поэтому начинается процесс замены HbF на гемоглобин взрослого типа HbA.
Методика диагностирования с использованием показателя гемоглобина F
Определение уровня белка HbF в организме имеет важное значение для диагностики различных заболеваний и состояний. Например, по его количеству можно судить о степени созревания и недоношенности ребенка.
Уровень HbF критичен при выявлении гемолитической анемии у новорожденных, особенно при проведении заменных переливаний крови. Заменное переливание осуществляется с использованием донорской крови, практически не содержащей HbF. Это позволяет оценить полноту переливания, так как количественный показатель HbF помогает определить его эффективность у новорожденного.
Определение уровня HbF также используется для диагностики анемии при гемотрансфузиях двух типов:
- фето-материнской;
- фето-фетальной.
При рождении ребенка с анемией у матери наблюдается повышение уровня HbF. Это указывает на фето-материнскую гемотрансфузию, когда красные кровяные клетки плода проникают в кровеносную систему матери. В случае близнецов анемия может развиться у одного из них. В этом случае уровень HbF помогает подтвердить или опровергнуть наличие фето-фетальной гемотрансфузии: один близнец будет иметь повышенный уровень HbF, а другой — пониженный.
Определение уровня HbF также является важным признаком при диагностике различных типов лейкозов. Повышение этого показателя может указывать на возвращение организма к эмбриональному типу кроветворения, что проявляется в появлении незрелых клеток крови.
Содержание HbF увеличивается при гипоксии и гипоксемии — нарушениях кислородоснабжения. Это происходит как компенсаторный механизм, способствующий синтезу HbF, обладающего повышенным сродством к кислороду.