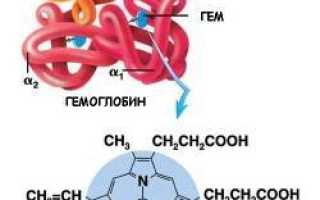
Функции гемоглобина (Hb) связаны с транспортировкой кислорода к тканям и органам. Гемоглобин (Hb) содержится в крови людей и животных. Эритроциты переносят кислород, связываясь с гемоглобином, к тканям.
Основные задачи
Железосодержащий белок выполняет свою функцию в три этапа:
- Присоединение молекул кислорода.
- Основная функция гемоглобина: молекула гемоглобина реагирует с кислородом, превращаясь в синглетный кислород, который может взаимодействовать с клетками организма.
- Доставка синглетного кислорода к тканям: гемоглобин связывается с кислородом в капиллярах легких, где его концентрация высокая. Эритроциты переносят соединения гемоглобина и кислорода к органам и тканям, испытывающим дефицит кислорода, высвобождая молекулы кислорода из связи с белком.
В организме здорового человека присутствует гемоглобин а, состоящий из белковой и небелковой частей. Он связывает небольшое количество CO2 (диоксид углерода) и освобождает его в легких. CO (монооксид углерода) образует более прочную связь с гемоглобином, чем кислород.
При этом образуется HbCO (карбоксигемоглобин). В результате некоторых процессов ионы железа в гемме могут окисляться до степени +3, образуя метгемоглобин. Эти формы блокируют транспортировку кислорода в организме.
Монооксид углерода можно частично вытеснить из геммы, увеличив парциальное давление кислорода в легких.
Мутационные процессы
Гемоглобин С отличается от нормального гемоглобина своей молекулярной структурой и физико-химическими свойствами. Его наличие в организме приводит к гемоглобинопатиям. При нарушении структуры гемоглобина рекомендуется исследовать кровь на наличие таких заболеваний, как талассемия и серповидно-клеточная анемия. Определить уровень гемоглобина (Hb) в крови можно с помощью следующих методов:
- измерение связываемого кислорода;
- анализ содержания железа (Fe);
- колориметрический метод с использованием гематина или Hb.
В первом методе уровень белка определяется путем встряхивания крови с воздухом, что приводит к образованию оксигемоглобина. Затем оксигемоглобин превращается в метгемоглобин с добавлением красной кровяной соли, что позволяет высвободить рыхло связанный кислород. Его количество измеряется с помощью аппарата Баркрофта или Ван Слайка.
Один из простых колориметрических методов — метод Сали. Для анализа берут 20 куб. мм крови с помощью микропипетки и разводят децинормальной HCl в градуированной пробирке до деления 10. Hb распадается на гемм и глобин. Гемм, реагируя с кислородом, превращается в гематин, придавая раствору светло-коричневый цвет.
Полученный цвет сравнивают со стандартом (раствор в запаянных пробирках аналогичного диаметра). Добавляют дистиллированную воду до достижения соответствия цвета пробы стандарту. Чем больше воды требуется, тем выше концентрация Hb. Пробирки имеют деления, показывающие процентное содержание гемоглобина относительно нормы. Метод Сали предполагает, что 100 % Hb соответствует 17,3 г/100 мл крови. У большинства здоровых пациентов этот показатель составляет 80–90 % (14–16 г/100 мл крови).
Причины определения количества Hb
Определение концентрации гемоглобина важно для диагностики и выявления патологий. Анализ на общий гемоглобин назначают при подозрении на анемию, а для диагностики сахарного диабета требуется биохимический анализ крови с определением уровня гликозированного Hb.
Нормальные значения для мужчин составляют 135-160 г/л, для женщин и детей — 120-140 г/л. Объем гликозированного Hb в организме составляет 4-6%.
Строение гемоглобина связано с его функциями.
Повышение концентрации гемоглобина в крови может указывать на патологии, вызывающие эритроцитоз (увеличение количества красных кровяных клеток). При этом формула и структура гемоглобина остаются неизменными.
Медики выделяют следующие типы патологий:
- Абсолютные — возникают при физиологических изменениях, приводящих к увеличению концентрации эритроцитов.
- Относительные — временные, возникают из-за обезвоживания или уменьшения объема плазмы.
- Истинные — связаны с эритремией или заболеваниями кроветворения, сопровождаются повышением давления, покраснением кожи, закупоркой сосудов и увеличением селезенки.
Причины повышения уровня Hb могут включать заболевания сердечно-сосудистой системы, гипоксию, ожирение, проживание в высокогорьях, курение, образование неактивного гемоглобина, чрезмерные физические нагрузки, стресс, обезвоживание, увеличение кортикостероидов и андрогенов, а также ожоги и отравления.
Самостоятельно понижать уровень Hb не рекомендуется. При его повышении необходимо определить причины, учитывая все функции гемоглобина, и провести диагностику для назначения адекватного лечения.
Пониженный уровень Hb
Уменьшение концентрации гемоглобина (анемия) может быть вызвано следующими факторами:
- снижение количества эритроцитов;
- значительная потеря крови;
- дефицит железа, витамина С, фолиевой кислоты или витамина В12;
- нарушения в развитии красных кровяных телец;
- отравление печени и ее дисфункция;
- вегетарианство или несбалансированное питание;
- острые и хронические инфекции;
- алкоголизм;
- коллагеноз;
- наследственность;
- чрезмерное употребление чая или кофе.
Анемия может развиваться после операций или во время беременности. У беременных уровень гемоглобина может снижаться до 110 г/л крови из-за повышенной потребности в микроэлементах как у женщины, так и у плода. Для определения уровня гемоглобина у беременной рекомендуется сдать анализ крови.
При низком уровне гемоглобина (Hb) рекомендуется принимать витамины группы В и препараты с высоким содержанием железа, а также скорректировать рацион. Диагностика анемии основывается на показателях Hb, так как уровень эритроцитов может оставаться нормальным на ранних стадиях.
Медики выделяют шесть типов анемии:
- железодефицитная — наиболее распространенная форма, возникающая из-за недостатка железа, которое организм не может вырабатывать самостоятельно;
- острая постгеморрагическая — возникает из-за значительной потери крови в результате операций, травм или внутренних кровотечений;
- анемия Аддисона-Бирмера (фолиеводефицитная);
- сидероахрестическая — связана с нарушением синтеза и утилизации порфирина и накоплением железа в организме, может быть наследственной или приобретенной, включая прием противотуберкулезных препаратов;
- угнетение пролиферации эритроидного ростка;
- гемолитическая — возникает из-за ускоренного распада эритроцитов.
Симптоматика анемии
Медики выделяют общие и специфические симптомы анемии. Специфические симптомы зависят от причины заболевания. Общие симптомы включают:
- потрескавшиеся губы и заеды в уголках рта;
- болезненный язык;
- сухая, бледная (иногда желтоватая) кожа;
- длительное заживление царапин;
- тусклые и секущиеся волосы;
- ломкие ногти;
- помутнение в глазах;
- снижение внимания;
- повышенная утомляемость;
- плохая переносимость душных помещений;
- мышечная слабость;
- депрессивные состояния;
- сонливость;
- ослабление иммунитета;
- частые позывы к мочеиспусканию;
- головокружение;
- слюнотечение по ночам;
- головные боли;
- учащенное сердцебиение;
- обмороки;
- одышка;
- увеличение селезенки или печени (не всегда).
Клинические проявления усиливаются по мере прогрессирования анемии. Биохимические анализы помогают понять реакции в организме. Строение и функции гемоглобина могут изменяться под воздействием патологических процессов. Дефицит железосодержащего белка не следует путать с гипоксемией (понижением кислорода в крови). Патологии костного мозга и почек, а также значительная потеря крови приводят к снижению концентрации гемоглобина, в то время как легочный фиброз и врожденные патологии сердца могут вызывать его повышение.
Вредные соединения
Hb может реагировать с угарным газом, образуя HHbCO, что снижает функциональные способности гемоглобина. Пребывание в помещениях с угарным газом опасно для жизни. Для соединения 80 % гемоглобина с СО достаточно вдыхать 0,1 % газа с кислородом. Курильщики подвергают свое здоровье серьезному риску, так как уровень HHbCO в их организме может превышать норму в 3-10 раз.
Замена Fe2+ на Fe3+ (двухвалентного на трехвалентное железо) также представляет опасность. Это приводит к образованию метгемоглобина, который замедляет доставку кислорода к органам. Отравление химикатами может вызвать метгемоглобинемию, которая может быть наследственной.
Hb становится токсичным при попадании из эритроцитов в плазму. Токсичность обусловлена:
- повышением концентрации продуктов распада;
- гипоксией тканей.
В организме существуют механизмы, которые связывают и нейтрализуют токсичные вещества. Нормальный уровень Hb у мужчин и женщин немного различается из-за физиологических особенностей.
Во время менструаций и беременности уровень гемоглобина снижается из-за разжижения крови. Средние нормы для женщин составляют 115-145 г/л (во время беременности — до 110 г/л), для мужчин — 130-160 г/л. Цветовые показатели указывают на насыщение крови:
- ниже 0,8 (анемия);
- 0,8 — 1,0 (норма);
- выше 1,0.
При необходимости медики могут определить содержание Hb в одном эритроците (норма — 27-31 пг). Также с помощью гематологического анализатора определяют средний объем красных кровяных телец, гематокрит, показатель гетерогенности эритроцитов и среднее количество Hb в эритроцитах.
Причины изменения уровня Hb
Количество гемоглобина в организме может изменяться из-за рациона, времени года (понижается осенью), образа жизни (физическая активность способствует повышению), рельефа местности и климата. Чистый воздух и курение также влияют на уровень гемоглобина, повышая его.
Перед тем как повышать уровень гемоглобина, важно определить причины его снижения. Для этого необходимо пройти комплекс обследований, включая фиброгастродуоденоскопию. Среди растительных продуктов много тех, что богаты железом, но они лучше усваиваются в сочетании с белками:
- говядина;
- телятина;
- куриные яйца.
Особенности диеты при анемии:
- Гречка — лучший гарнир, овсяные хлопья и пшенная каша занимают второе место.
- Аскорбиновая кислота способствует усвоению железа, поэтому в рацион включают цитрусовые.
- Крепкий чай после еды заменяют на какао на воде, настой шиповника или черный шоколад.
- Продукты с высоким содержанием кальция мешают усвоению железа.
- Небольшое количество сухого красного вина.
- Гематоген.
Включение в рацион продуктов, богатых железом, помогает справиться с легкой формой анемии. При выраженной форме может потребоваться прием железосодержащих препаратов, которые должен назначить врач на основе анализов и индивидуальных особенностей пациента.
Источник: osostavekrovi.ru
Строение
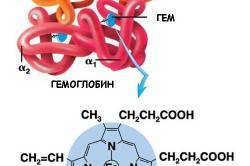
Гемоглобин — это сложный белок класса хромопротеинов, содержащий пигментную группу гем, в состав которой входит железо. Он представляет собой тетрамер, состоящий из четырёх субъединиц: α1, α2, β1 и β2. Субъединицы соединены по принципу изологического тетраэдра, и основную роль в их взаимодействии играют гидрофобные связи. Обе цепи, α и β, относятся к α-спиральному структурному классу и содержат восемь спиральных участков, обозначаемых буквами A-H (от N-конца к C-концу).
Гем — это комплекс протопорфирина IX с атомом железа(II). Эта простетическая группа нековалентно связана с гидрофобной впадиной молекул гемоглобина и миоглобина.
Железо(II) имеет октаэдрическую координацию и связывается с шестью лигандами. Четыре из них — это атомы азота порфиринового кольца, находящиеся в одной плоскости. Две другие координационные позиции расположены на оси, перпендикулярной плоскости порфирина. Одна из них занята азотом остатка гистидина в 93-м положении полипептидной цепи (участок F). Связываемая гемоглобином молекула кислорода координируется к железу с обратной стороны и оказывается между атомом железа и азотом другого остатка гистидина в 64-м положении цепи (участок E).
В гемоглобине человека четыре участка связывания кислорода (по одному гему на каждую субъединицу), что позволяет связываться четырём молекулам кислорода одновременно. В легких, при высоком парциальном давлении кислорода, гемоглобин образует оксигемоглобин, связываясь с кислородом через 6-ю координационную связь. На эту же связь может присоединяться и моноксид углерода, который конкурирует с кислородом за связывание с гемоглобином, образуя карбоксигемоглобин.
Связь моноксида углерода с гемоглобином прочнее, чем с кислородом, что приводит к тому, что часть гемоглобина, образующая комплекс с моноксидом углерода, не участвует в транспорте кислорода. В норме у человека образуется 1,2% карбоксигемоглобина, а его повышенный уровень указывает на гемолитические процессы, что делает его показателем гемолиза.
Физиология
Связывание кислорода с гемоглобином характеризуется кооперативностью: после присоединения первой молекулы кислорода связывание последующих облегчается.
Гемоглобин является основным белком, который используют малярийные плазмодии — возбудители малярии. В эндемичных районах распространены наследственные аномалии гемоглобина, затрудняющие питание плазмодиев и их проникновение в эритроциты. Одной из таких мутаций, имеющей эволюционно-приспособительное значение, является аномалия, приводящая к серповидно-клеточной анемии. Однако эти аномалии, как и другие, не имеющие явного приспособительного значения, нарушают кислород-транспортирующую функцию гемоглобина, снижают устойчивость эритроцитов к разрушению и приводят к анемии и другим негативным последствиям. Аномалии строения гемоглобина называют гемоглобинопатиями.
Гемоглобин становится высоко токсичным при попадании в плазму крови в значительных количествах, что происходит при массивном гемолизе, геморрагическом шоке, гемолитических анемиях, переливании несовместимой крови и других патологических состояниях. Токсичность свободного гемоглобина проявляется в тканевой гипоксии — ухудшении кислородного снабжения тканей, перегрузке организма продуктами его разрушения (железом, билирубином, порфиринами), что может привести к желтухе или острой порфирии. Также возможна закупорка почечных канальцев крупными молекулами гемоглобина, что вызывает некроз и острую почечную недостаточность.
Из-за высокой токсичности свободного гемоглобина в организме существуют специальные системы для его связывания и обезвреживания. Одним из компонентов этой системы является плазменный белок гаптоглобин, который специфически связывает свободный глобин и глобин в составе гемоглобина. Комплекс гаптоглобина и глобина затем захватывается селезёнкой и макрофагами тканевой ретикуло-эндотелиальной системы для обезвреживания.
Другой частью системы обезвреживания гемоглобина является белок гемопексин, который связывает свободный гем и гем в составе гемоглобина. Комплекс гемопексина с гемом (или гемоглобином) захватывается печенью, где гем отщепляется и используется для синтеза билирубина и других желчных пигментов или возвращается в рециркуляцию в комплексе с трансферрином для повторного использования в костном мозге в процессе эритропоэза.
Гемоглобин при заболеваниях крови
Дефицит гемоглобина может возникать по двум причинам: во-первых, из-за уменьшения количества молекул гемоглобина (анемия), во-вторых, из-за сниженной способности каждой молекулы связывать кислород при том же парциальном давлении.
Гипоксемия — это снижение парциального давления кислорода в крови, и её следует отличать от дефицита гемоглобина. Оба состояния могут приводить к гипоксии.
Причины низкого уровня гемоглобина разнообразны: кровопотеря, нехватка питательных веществ, заболевания костного мозга, химиотерапия, почечная недостаточность и атипичный гемоглобин.
Повышенное содержание гемоглобина в крови связано с увеличением количества или размеров эритроцитов, что наблюдается при полицитемии. Это может быть вызвано врожденными заболеваниями сердца, легочным фиброзом или избытком эритропоэтина.
См. также
- Гемоглобин А
- Гемоглобин С (мутантная форма)
- Гемоглобин E (эмбриональный)
- Гемоглобин S (мутантная форма)
- Гемоглобин F (фетальный)
- Анемия
- Порфирия
- Талассемия
- Вериго-Бора эффект
Гемоглобин (от греч. haima — кровь и лат. globus — шар) — сложный железосодержащий белок эритроцитов, который связывается с кислородом и переносит его в ткани.
Основная функция гемоглобина — транспортировка дыхательных газов. В капиллярах легких кислород соединяется с гемоглобином. Эритроциты, содержащие кислород, доставляются к органам и тканям, где кислорода мало, и здесь он освобождается для окислительных процессов. Гемоглобин также связывает небольшое количество углекислого газа (CO2) в тканях и освобождает его в легких. Монооксид углерода (CO) связывается с гемоглобином прочнее, чем кислород, образуя метгемоглобин (metHb), что блокирует транспортировку кислорода. В метгемоглобине железо находится в трехвалентном состоянии.
Нормальное содержание гемоглобина в крови: у мужчин — 130—170 г/л, у женщин — 120—150 г/л, у детей — 120—140 г/л.
Гемоглобин относится к хромопротеинам, где простетической группой является гем, содержащий железо. Молекула гемоглобина состоит из четырех полипептидных цепей, каждая из которых связана с гемом.
Гемоглобин является основным белком, необходимым для питания плазмодиев малярии. В районах с высокой заболеваемостью малярией распространены наследственные аномалии гемоглобина, которые затрудняют плазмодиям доступ к этому белку. Одной из таких аномалий является серповидно-клеточная анемия. Однако эти аномалии могут нарушать кислородно-транспортную функцию гемоглобина, снижать устойчивость эритроцитов и вызывать анемию. Аномалии строения гемоглобина называются гемоглобинопатиями.
Свободный гемоглобин высоко токсичен при попадании в плазму крови, что может происходить при массивном гемолизе, геморрагическом шоке, гемолитических анемиях или переливании несовместимой крови. Токсичность свободного гемоглобина проявляется в тканевой гипоксии, перегрузке организма продуктами его разрушения (железом, билирубином, порфиринами), что может привести к желтухе, острой порфирии и почечной недостаточности.
Для связывания и обезвреживания свободного гемоглобина в организме существуют специальные системы. Одним из компонентов является плазменный белок гаптоглобин, который связывает свободный глобин. Комплекс гаптоглобина с глобином захватывается селезенкой и макрофагами, где он обезвреживается.
Другим компонентом системы является гемопексин, который связывает свободный гем. Комплекс гемопексина с гемом захватывается печенью, где гем используется для синтеза билирубина и других желчных пигментов или возвращается в кровоток для повторного использования в эритропоэзе.