Гепатит C генотип 3
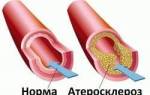
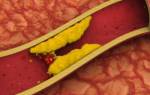
Гепатит С — вирусное заболевание, подверженное постоянным мутациям. Эти изменения мешают организму выработать иммунитет и эффективно бороться с инфекцией. Генотип 3 является одним из наиболее распространённых среди всех разновидностей вируса гепатита С. В природе существует ещё 5 типов вируса, а генотип 3 включает 6 подтипов.
Что означает гепатит С генотип 3 и как передается
Третий генотип вируса гепатита C отличается высокой устойчивостью к медикаментозной терапии. Наиболее распространены подтипы 3a и 3b. Генотип 3a чаще передается половым путем, поражает билиарную систему, но реже вызывает рак печени.
Вирус передается через кровь. Инфицироваться им можно в следующих случаях:
- маникюр вне дома без соблюдения стерильности;
- незащищенный половой акт;
- татуировки с использованием нестерилизованных инструментов;
- стоматологические процедуры без соблюдения стерильности;
- переливание крови;
- наркотические инъекции с использованием общей иглы.
Его симптомы и отличие от других штаммов
Заболевание проявляется стандартными симптомами:
- плохое самочувствие;
- высокая утомляемость;
- снижение рабочей активности;
- субфебрильная температура;
- увеличение объема печени;
- боли в суставах;
- кожный зуд;
- изменение цвета кала на светлый;
- мигрени;
- лихорадка;
- боль в правом боку;
- механическая желтуха;
- потемнение мочи.
Гепатит с генотипом 3а также может вызывать тошноту, потерю аппетита, рвоту и резкое снижение массы тела.
Главной особенностью этого штамма является длительный латентный период. Симптомы могут не проявляться в течение нескольких лет, что затрудняет диагностику и выбор эффективного лечения.
Диагностика и лечение
Для правильного лечения патологии необходимо сначала установить тип вируса и оценить общее состояние организма. Для этого применяются следующие диагностические методы:
- Биохимический анализ крови для определения изменений в показателях аспартатаминотрансферазы, щелочной фосфатазы, аланинаминотрансферазы и билирубина.
- Полимеразная цепная реакция (ПЦР) для выявления рибонуклеиновой кислоты в биоматериале.
- Биопсия печени для подтверждения цирроза.
- Рентгенография органа.
- Общий анализ крови для выявления анемии и других сопутствующих заболеваний.
- Иммуноферментный анализ для обнаружения антител к вирусным антигенам или антигенов к антителам.
- Фиброгастродуоденоскопия.
- Ультразвуковое исследование органов брюшной полости для оценки объема, структуры печени и состояния ее кровоснабжения.
- Гистологическое исследование для определения стадии фиброза.
- Эластография для оценки параметров фиброзного процесса.
- Электрокардиография.
- Сцинтиграфия.
Ранее считалось, что успешность лечения третьего типа зависит от стадии цирроза: при обширном поражении летальный исход был неизбежен. Однако современные методы медицины позволяют достигать устойчивой ремиссии и иммунного ответа даже при значительном поражении печени.
Современные медикаменты, подавляющие вирус, обеспечивают высокий процент успешного исхода терапии в течение года. Однако лечение гепатита с 3а ингибиторами протеазы неэффективно, хотя эти препараты хорошо работают с другими штаммами.
Наиболее эффективным считается сочетание Рибавирина и интерферона, которые замедляют размножение вируса. Также распространен прием Рибавирина вместе с полиэтиленгликолиевым интерфероном Пегасис, что помогает снизить побочные эффекты.
Популярен двухнедельный курс лечения Копегусом и Пегасисом. Дозировка Копегуса назначается врачом в зависимости от индивидуальных показателей пациента, а пегинтерферон применяется по 180 мг ежедневно.
Для дополнительного лечения используются антигистаминные препараты, витаминные комплексы, сорбенты и гепатопротекторы.
Цена каждого из указанных препаратов редко превышает тысячу рублей.
Эти схемы терапии позволяют достичь полного выздоровления почти в 90% случаев заболевания.
Осложнения
В большинстве случаев заболевание удается диагностировать слишком поздно. Пациенты обращаются к врачу только при появлении ярких признаков осложнений. После обращения к специалисту становится понятно, как протекает заболевание. Осложнения, такие как цирроз, стеатоз или фиброз, свидетельствуют о необратимых изменениях в организме, которые трудно поддаются восстановлению. Поэтому врачи подчеркивают важность раннего выявления заболевания и начала лечения.
Цирроз проявляется в необратимом замещении паренхиматозной ткани, что нарушает функции печени и приводит к печеночной недостаточности и портальной гипертензии. У пациента могут развиваться следующие симптомы печеночной недостаточности:
- отеки на ногах;
- асцит;
- ухудшение аппетита;
- повышенная утомляемость;
- ослабление иммунитета;
- боли в правом подреберье;
- частые вздутия;
- кровоизлияния и синяки на коже.
Стеатоз характеризуется избыточным накоплением липидов в клетках печени. Он прогрессирует медленно и часто бессимптомно, его можно выявить случайно при ультразвуковом исследовании. Однако некоторые симптомы могут указывать на наличие стеатоза:
- тошнота;
- частая слабость;
- тяжесть в желудке.
Фиброз — одна из форм онкопатологии, чаще встречающаяся у мужчин, но также диагностируемая у женщин. Без быстрого лечения риск прогрессирования заболевания велик. Явные признаки патологии включают:
- механическую желтуху;
- снижение массы тела;
- отсутствие аппетита;
- увеличение объема печени;
- опухоль;
- тошноту.
При криоглобулинемии, когда иммуноглобулины выпадают в осадок при снижении температуры крови ниже 37 градусов, поражаются практически все внутренние органы. Симптомы включают:
- синдром Рейно — вазоспастическое заболевание, проявляющееся пароксизмальным нарушением артериального кровообращения в конечностях под воздействием холода или эмоционального стресса;
- артралгии — боли в суставах, имеющие переменный характер;
- гепатоспленомегалия — одновременное увеличение печени и селезенки;
- почечную недостаточность.
Продолжительность жизни при такой патологии зависит от штамма вируса и стадии поражения. Риск неблагоприятного исхода значительно возрастает у людей, злоупотребляющих алкоголем. При адекватной терапии в 90% случаев возможно полное излечение и возвращение к нормальной жизни.
Видео
Генотипы гепатита C
В медицине гепатит C считается одним из самых серьезных диагнозов, не поддающимся эффективному лечению. Вакцинация против вируса находится на стадии разработки, а по тяжести и исходам заболевание сравнивают со СПИДом.
При гепатите C происходит массовая гибель печеночных клеток и образование обширных некротических очагов в печени. Однако клиническая картина заболевания варьируется. Это связано с тем, что генотипы вируса гепатита C имеют свои особенности и специфику воздействия на организм человека.
Какие известны генотипы гепатита
- 1a, 1b, 1c
- 2a, 2b, 2c, 2d
- 4a, 4b, 4c, 4d, 4e, 4f, 4g, 4h, 4i, 4
- 5a
- 6a
В чем заключается опасность генотипов
При наличии одного вируса в организме, проникновение другого приводит к ухудшению прогноза заболевания и повышает риск цирроза печени. Определить тип вируса можно только с помощью лабораторных тестов на генотипы.
Источник: gepatit.lechenie-pechen.ru
Гепатоцеллюлярная карцинома
Ежегодно от гепатоцеллюлярной карциномы (ГЦК) умирает 1,25 миллиона человек. Эта опухоль занимает седьмое место среди всех злокачественных новообразований. Распространённость ГЦК варьируется в зависимости от географического региона. Наиболее часто она встречается у жителей Африки и Азии, где почти всегда развивается на фоне цирроза печени. В странах Юго-Восточной Азии ГЦК является второй по распространённости злокачественной опухолью. Частота случаев заболевания также растёт в западных странах, что, вероятно, связано с распространением вирусного гепатита В и С, являющихся основными причинами развития ГЦК.
Экспериментальный рак печени
Существует множество канцерогенов, способных вызывать опухоли у животных в экспериментах, однако их роль в развитии опухолей у человека не установлена. К таким канцерогенам относятся р-диметиламиноазобензол (жёлтая краска), нитрозамины, афлатоксин и алкалоиды крестовника.
Процесс канцерогенеза включает несколько стадий, начиная с инициации и заканчивая прогрессией и клиническими проявлениями. Канцероген связывается с ДНК ковалентными связями. Развитие рака зависит от способности клеток хозяина к репарации ДНК и толерантности к канцерогенезу.
Связь с циррозом печени
Цирроз, независимо от причины, может считаться предраковым состоянием. Узловая гиперплазия может прогрессировать в рак. Дисплазия гепатоцитов, проявляющаяся увеличением размеров клеток, ядерным полиморфизмом и наличием многоядерных клеток, затрагивает группы клеток или целые узлы и может быть промежуточной стадией опухоли. Дисплазия наблюдается у 60% пациентов с гепатоцеллюлярной карциномой (ГЦК) на фоне цирроза печени и лишь у 10% пациентов с ГЦК без цирроза. При циррозе с высокой пролиферативной активностью гепатоцитов риск развития рака печени возрастает. Кроме того, канцерогенез может быть связан с генетическим дефектом определённого клона клеток.
В одном из исследований, включавшем 1073 пациента с ГЦК, у 658 (61,3%) был выявлен цирроз печени. Однако у 30% африканцев с ГЦК, ассоциированной с гепатитом В, цирроз отсутствовал. В Великобритании примерно у 30% пациентов с ГЦК не было цирроза; продолжительность жизни в этой группе была сравнительно высокой.
Существуют значительные географические различия в частоте рака среди пациентов с циррозом печени. Особенно высокая частота наблюдается в Южной Африке и Индонезии, где рак развивается более чем у 30% больных циррозом, в то время как в Индии, Великобритании и Северной Америке этот показатель составляет около 10-20%.
Связь с вирусами
При вирусном поражении печени гепатоцеллюлярная карцинома (ГЦК) развивается на фоне хронического гепатита и цирроза. Почти у всех пациентов с вирусассоциированной ГЦК наблюдается сопутствующий цирроз. Некроз и повышенная митотическая активность гепатоцитов способствуют образованию узлов регенерации, что может привести к дисплазии гепатоцитов и развитию рака. Хотя чаще всего рак предшествует узловой регенерации и циррозу, опухоль может возникнуть и без цирроза. В таких случаях, как при хроническом гепатите сурков (вызываемом вирусом, близким к вирусу гепатита В), необходимыми условиями для развития рака являются некроз и воспаление.
Связь с вирусом гепатита В
По данным мировой статистики, носительство HBV связано с заболеваемостью гепатоцеллюлярной карциномой (ГЦК). Наибольшая частота ГЦК наблюдается в странах с высоким уровнем носителей HBV. Риск развития ГЦК у носителей HBV выше, чем в общей популяции. Также установлена этиологическая роль других гепаднавирусов, например, вируса гепатита сурков. В тканях ГЦК обнаруживается HBV-ДНК.
Канцерогенез — многостадийный процесс, в котором участвуют как вирус, так и организм хозяина. Результатом этого процесса является дезорганизация и перестройка ДНК гепатоцитов. При гепатите В вирус интегрируется в хромосомную ДНК хозяина, но молекулярный механизм канцерогенного действия HBV остается неясным. Интеграция сопровождается хромосомными делециями и транслокациями, влияющими на рост и дифференцировку клеток (инсерционный мутагенез). Однако делеции не совпадают с участками встраивания вирусной ДНК, и в 15% случаев рака последовательности вирусного генома в опухолевой ткани не обнаруживаются. Встраивание HBV-ДНК в геном хозяина не приводит к повышенной экспрессии определенных протоонкогенов или делециям специфических участков генома, содержащих потенциальные антионкогены. Характер интеграции вирусного генома в клетки хозяина варьируется, и у разных пациентов он может происходить в различных участках ДНК опухолевых клеток.
Х-антиген HBV считается трансактиватором, который увеличивает скорость транскрипции онкогенов.
Пре-S-белок оболочки HBV может накапливаться в токсических количествах, способствующих развитию опухолей. Повышенное образование пре-S-белка у трансгенных мышей вызывает тяжелое воспаление печени и регенерацию, что может привести к опухолям. Нарушение регуляции экспрессии белков оболочки HBV может быть следствием интеграции в ДНК клеток хозяина.
Интеграция HBV-ДНК приводит к транслокации генов-супрессоров опухоли на хромосоме 17. Гены супрессии опухоли, такие как онкоген р53, могут играть важную роль в HBV-зависимом гепатоканцерогенезе. Трансформирующий фактор роста альфа (ТФР-а) активно экспрессируется у 80% пациентов с ГЦК и может выступать в роли кофактора. Гистохимические исследования показывают, что ТФР-а локализуется в тех же гепатоцитах, что и HBsAg, но отсутствует в опухолевых клетках.
Хронический гепатит В с развитием цирроза имеет наибольшее значение как предраковое состояние. HBV способствует развитию рака через интеграцию, трансактивацию, мутации генов-супрессоров и повышение уровня ТФР-а.
У носителей HBsAg, инфицированных HDV, ГЦК встречается реже, возможно, из-за подавляющего действия HDV.
Связь с вирусом гепатита С
Существует четкая связь между частотой инфицирования HCV и распространенностью гепатоцеллюлярной карциномы (ГЦК). В Японии у большинства пациентов с ГЦК в сыворотке крови обнаруживаются анти-НСV-антитела, и примерно в половине случаев имеется история гемотрансфузий. Аналогичная корреляция наблюдается в Италии, Испании, Южной Африке и США. В регионах, где распространена HBV-инфекция, например, в Гонконге, значение HCV в развитии ГЦК невелико. Внедрение более точных методов диагностики HCV-инфекции, чем тесты первого поколения, повлияло на результаты эпидемиологических исследований. Например, частота HCV-инфекции при ГЦК в Южной Африке составила не 46,1%, а 19,5%. В США у 43% пациентов с ГЦК (HBsAg-отрицательных) выявляют анти-HCV с помощью тест-систем второго поколения или HCV-РНК в сыворотке крови и печени. HCV, вероятно, играет более значимую роль в развитии ГЦК, чем HBV. Частота ГЦК среди пациентов с анти-HCV в 4 раза выше, чем у носителей HBsAg. Развитие ГЦК при HCV-инфекции не зависит от генотипа вируса.
Низкая частота ГЦК, связанной с HCV, в США по сравнению с Японией объясняется возрастом пациентов. ГЦК развивается через 10-29 лет после инфицирования. В Японии HCV-инфицирование, вероятно, происходило в раннем детском возрасте из-за инъекций с нестерильными шприцами. В США инфицирование происходило в основном во взрослом возрасте (через наркоманию и гемотрансфузии), что не позволяло ГЦК развиться в течение жизни.
В отличие от HBV, HCV является РНК-содержащим вирусом, не имеет фермента обратной транскриптазы и не может интегрироваться в геном клеток хозяина. Процесс развития ГЦК остается неясным; предполагается, что он происходит на фоне цирротической трансформации печени. Однако геном HCV можно обнаружить в опухолях и окружающей печеночной ткани этих пациентов.
Существует возможность взаимодействия HBV и HCV в развитии ГЦК, так как у пациентов с коинфекцией HCV и HBV (HBsAg-положительных) ГЦК развивается чаще, чем у тех, кто имеет только анти-HCV.
Носители HCV, как и носители HBV, должны регулярно проходить обследование на наличие ГЦК с помощью ультразвукового исследования (УЗИ) и определения уровня α-фетопротеина (α-ФП) в сыворотке крови.
Связь с употреблением алкоголя
В Северной Европе и Северной Америке риск развития первичной гепатоцеллюлярной карциномы (ГЦК) в 4 раза выше у пациентов с алкоголизмом, особенно пожилого возраста. У таких больных всегда наблюдаются признаки цирроза, хотя алкоголь сам по себе не является печёночным канцерогеном.
Алкоголь может выступать в роли коканцерогена при инфекциях вирусом гепатита B (HBV). У пациентов с алкогольным циррозом и ГЦК часто выявляют маркёры гепатита B. Стимуляция ферментов алкоголем может усиливать превращение коканцерогенов в канцерогены. Кроме того, алкоголь может способствовать канцерогенезу за счёт угнетения иммунной системы и замедления алкилирования ДНК, вызванного канцерогенами.
При ГЦК у больных с алкогольным циррозом иногда обнаруживают встроенную в ДНК перерождённых гепатоцитов ДНК HBV. Однако ГЦК может развиваться у пациентов с алкоголизмом и без текущей или перенесённой ранее HBV-инфекции.
Микотоксины
Наибольшее значение среди микотоксинов имеет афлатоксин, вырабатываемый плесневым грибком Aspergillus flavis. Он вызывает выраженный канцерогенный эффект у радужной форели, мышей, морских свинок и обезьян. Чувствительность к канцерогенному действию афлатоксина варьируется между видами. Афлатоксин и другие токсичные вещества из плесени могут легко попасть в продукты питания, особенно в земляные орехи (арахис) и зерновые культуры, если они хранятся в тропических условиях.
В различных районах Африки наблюдается положительная корреляция между содержанием афлатоксина в пище и частотой возникновения гепатоцеллюлярной карциномы (ГЦК). Афлатоксин может действовать как коканцероген при вирусном гепатите В.
Исследования в Мозамбике, Южной Африке и Китае выявили мутации гена супрессии опухолей р53, связанные с повышенным содержанием афлатоксина в пищевых продуктах. В Великобритании, где вероятность попадания афлатоксина в продукты низка, такие мутации у больных со злокачественными опухолями печени встречаются редко.
Расовая принадлежность и пол
Доказательства генетической предрасположенности к развитию ГЦК отсутствуют.
ГЦК у мужчин встречается в три раза чаще, чем у женщин. Это можно частично объяснить более высокой частотой носительства HBV среди мужчин. Возможно, это связано с усилением экспрессии рецепторов андрогенов и подавлением рецепторов эстрогенов в опухолевых клетках. Биологическое значение данного явления остается неясным.
Заключение
Вирусы гепатита В и С, при участии различных кофакторов, играют ключевую роль в развитии гепатоцеллюлярной карциномы (ГЦК) по всему миру. Однако в регионах с низкой распространённостью этих вирусов причиной опухоли могут быть другие факторы. В таких случаях механизм канцерогенеза и роль цирроза печени в развитии опухоли остаются неясными.